روی
روی (به انگلیسی: Zinc) عنصری است شیمیایی با علامت اختصاری Zn که دارای عدد اتمی ۳۰ است. روی فلزی است به رنگ سفید متمایل به آبی که بر اثر رطوبت هوا تیره رنگ میشود و در حین احتراق رنگ سبز براقی تولید میکند. روی بعد از آهن، آلومینیوم و مس چهارمین فلز مورد استفاده در دنیا میباشد. از موارد استفاده روی میتوان آلیاژهای مختلف از جمله برنج و فولاد گالوانیزه را نام برد.
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| روی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ظاهر | نقره-gray | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| جرم اتمی استاندارد (Ar، استاندارد) | ۶۵٫۳۸(۲)[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| روی در جدول تناوبی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اتمی (Z) | 30 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| گروه | گروه ۱۲ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دوره | دوره 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| بلوک | بلوک-d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دسته | Post-transition metal | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| آرایش الکترونی | [Ar] 3d10 4s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2, 8, 18, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای فیزیکی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| فاز در STP | جامد | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه ذوب | 692.68 K (419.53 °C, 787.15 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه جوش | 1180 K (907 °C, 1665 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| چگالی (near r.t.) | 7.14 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| در حالت مایع (at m.p.) | 6.57 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حرارت همجوشی | 7.32 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| آنتالپی تبخیر | 123.6 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ظرفیت حرارتی مولی | 25.470 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
فشار بخار
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای اتمی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اکسایش | −2, 0, +1, +2 (an amphoteric اکسید) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الکترونگاتیوی | مقیاس پائولینگ: 1.65 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| انرژی یونش |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع اتمی | empirical: 134 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع کووالانسی | pm 122±4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع واندروالسی | 139 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Color lines in a spectral range | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دیگر ویژگی ها | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ساختار بلوری | دستگاه بلوری ششگوشه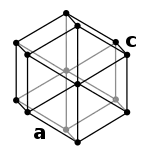 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سرعت صوت thin rod | (rolled) 3850 m/s (at r.t.) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| انبساط حرارتی | 30.2 µm/(m·K) (at 25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانندگی گرمایی | 116 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانش الکتریکی | 59.0 n Ω·m (at 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانش مغناطیسی | diamagnetic | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول یانگ | 108 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول برشی | 43 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول حجمی | 70 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نسبت پواسون | 0.25 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سختی موس | 2.5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سختی برینل | 412 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شماره ثبت سیایاس | 7440-66-6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ایزوتوپهای روی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
تاریخچه
آلیاژهایی که روی در آن ها قرار میگیرد از قرنها پیش استفاده میشدهاست. کالاهای برنجی که به ۱۰۰۰–۱۴۰۰ سال پیش بازمیگردند در فلسطین پیدا شدهاند و اشیاء رویی با ۸۷٪ روی در ترانسیلوانیا ما قبل تاریخ یافت شدهاند. به خاطر نقطه جوش پایین و واکنش شیمیایی این فلز (روی جدا شده دود شده و قابل دست یابی نبود) خصوصیات واقعی این فلز در زمان باستان مشخص نشده بود. ساخت برنج به رومیها نسبت داده شده و مربوط به ۳۰ سال پیش از میلاد میباشد. آنها کالامین و مس را با یکدیگر در بوته آهنگری حرارت میدادند که در این عمل اکسید روی در کالامین کاهش میافت و فلز روی آزاد توسط مس به دام انداخته میشد و به شکل آلیاژ درمیآمد. برنج بدست آمده یا در قالب ریخته میشد یا با چکش به شکلهای مختلف درمیآمد.

استخراج و تصفیه روی نا خالص در ۱۰۰۰ سال پیش از میلاد مسیح در هند و چین صورت میگرفتهاست. در غرب نیز کشف فلز روی به Andreas Marggraf آلمانی در سال ۱۷۴۶ بر میگردد.
شرح تولید برنج در اروپای غربی در کتابهای آلبرتوس مگنوس در سال ۱۲۸۴ به چشم میخورد. این فلز در قرن ۱۶ به میزان قابل توجه شناخته شد. Agricola در سال ۱۵۴۶ اعلام کرد که وقتی که سنگ معدن روی گداخته میشود فلز سفید میتواند منقبض شود و دیواره کوره را بتراشد. او در نوشتههای خود به این مسئله نیز اشاره کرد که فلزی شبیه آن به نام Zincum در Silesia تولید میشدهاست. پاراسلیوس (متوفی به سال ۱۵۴۱) اولین کسی در غرب بود که گفت Zircum فلزی جدید است که در مقایسه با فلزات دیگر خواص شیمیایی جداگانهای دارد. نتیجه آن است که فلز روی زمانی شناخته شده که Margaraf کشفیاتش را شروع کرد و در حقیقت فلز روی دو سال زودتر توسط شیمیدان دیگری به نام Anton Von Swab تجزیه شده و بدست آمده بود. اما تحقیقات Margraaf جامع تر بود و بخاطر تحقیقات این دو شخص آنها به عنوان کاشفین روی شناخته میشوند.
قبل از کشف تکنیک غوطه وری سولفید روی Calamine تنها منبع معدنی فلز روی بودهاست.
خصوصیات قابل توجه
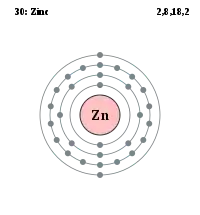
وزن اتمی۶۵٫۳۸ چگالی ۷٫۱۳۳ نقطه ذوب۴۱۹٫۸۳ درجه سانتیگراددرجه سختی بر حسب واحد موهس ۵/۲ دارای ظرفیت۲ درگروهIIB جدول تناوب دارای ایزوتوپهای طبیعی۷۰ -۶۸-۶۶-۶۴ وایزوتوپهای رادیواکتیو۷۲-۷۱-۶۹-۶۵-۶۳-۶۰ روی فلز نرم و سفیدباقابلیت چکش خواری باجلای خاکستری متمایل به آبی قابل حل دراسیدهاوبازهاوغیرقابل حل درآب میباشد.[2]
روی فلزی است که در Vielle Montagne و Zinkgruvan استخراج میشود و برای آبکاری الکتریکی فولاد مورد استفاده قرار میگیرد. مانند فلزات دیگر به آرامی واکنش نشان میدهد. با اکسیژن و دیگر غیر فلزات ترکیب شده و با اسید رقیق واکنش نشان داده و گاز هیدروژن آزاد میکند. چهارمین فلز متداول و مورد استفاده بوده و بعد از آهن آلومینیوم و مس بیشترین فلزی تولیدی میباشد. حالت اکسیداسیون متداول این عنصر +۲ میباشد.
کاربردها
روی برای آبکاری الکتریکی فلزها استفاده میشود تا از زنگ زدگی آنها جلوگیری کند. روی در آلیاژهایی نظیر برنج، ورشو، فلز ماشین تحریر، فرمولهای مختلف لحیم و… بکار میرود.
روی بهطور گسترده در صنعت خودروسازی در ریختهگری تحت فشار (دایکست) استفاده میشود. روی لولهای به عنوان قسمتی از محتوی باتریها مورد استفاده قرار میگیرد.
در سپتامبر سال 2020 محققان دانشگاه میشیگان اعلام کردند موفق به ساخت یک باتری از جنس روی شدهاند که بسیار قدرتمندتر از باتری لیتومی است. به علاوه با محیط زیست سازگار بوده و به راحتی بازیافت میشود و در ساخت رباتهای کارآمدتر نقش مهمی ایفا خواهد نمود[3].
از این فلز برای گالوانیزه کاری آهن، تولید ظروف، صنایع نظامی، خودروسازی، کشتی سازی، باتری سازی و تولید آلیاژ برنج استفاده می شود. برنج بخاطر استحکام و مقاومت در برابر زنگ زدگی و خوردگی کاربردهای وسیعی دارد. از آنجا که آلیاژ برنج در برابر زنگ زدگی و خوردگی مقاومت بالایی دارد می توان از آن در بسیاری از صنایع استفاده نمود. همچنین فلز روی جهت تولید مشتقات خالص خود همچون اکسید روی، کلرید روی، کربنات روی، نیترات روی و سولفات روی استفاده می شود.
اکسید روی به عنوان رنگدانههای سفید در رنگهای آبی و همچنین به عنوان فعالکننده در صنعت لاستیک استفاده میشود. به عنوان کرم (بدون نیاز به تجویز پزشک) به صورت لایه نازکی بر روی پوست بی حفاظ صورت و بینی استفاده میشود تا از کم شدن آب پوست جلوگیری کرده و در برابر آفتاب سوختگی در تابستان و باد زدگی در زمستان از پوست محافظت کند. استفاده از آن برای کودکان در هر مرحله از عوض کردن کهنه کودک توصیه شده زیرا از تحریکات پوستی جلوگیری میکند. کلرید روی به عنوان بوگیر و همچنین محافظ چوب نیز مورد استفاده قرار میگیرد. سولفید روی در رنگدانههای درخشان، برای تولید عقربههای ساعت و موارد دیگری که در تاریکی میدرخشد استفاده میشود.

محلولهای ضدعفونیکنندهای که از Calamine ساخته شده و ترکیبی از Zn-Hydroxy-Carbonate و سیلیکات است برای درمان جوشهای پوستی استفاده میشود. فلز روی شامل ویتامینهای مورد مصرف روزانه و مواد معدنی نیز میباشد و با توجه به فلزات دیگر این فلز دارای خاصیت ضد اکسیداسیون است که از پیری زود رس پوست و مفصلهای بدن محافظت میکند. با بررسی خواص روی به این نتیجه رسیدهاند که این عنصر میتواند به بهبودی بعد از عمل جراحی سرعت بخشد. Zinc Gluconate Glycine از قرصهای مکیدنی برای درمان سرما خوردگی و التهاب دهان و لوزهها میباشد.
نقش روی در تغذیه گیاهی
روی از جمله عناصر کم مصرف برای گیاهان است. این عنصر در ساختمان اسید آمینه تریپتوفان که پیش ماده سنتز اکسین است شرکت دارد و همچنین به همراه مواد پر مصرف ازجمله ازت و فسفر در تشکیل یاختههای اولیه گل دخالت دارد. روی در کانیهای خاک به صورت قابل تبادل در کلوئیدهای رس و هوموس یافت میشود. با افزایش pH و قلیایی شدن خاک، جذب شدن سطحی آن افزایش یافته و مقدار این عنصر در محلول خاک کاهش مییابدو شعاع یونی روی شبیه آهن (فرو) و منیزیم بوده و میتواند تا حدودی جایگزین این یونها شود. روی به صورت فعال جذب میشود، یون مس به شدت از جذب روی جلوگیری میکند و همچنین فسفر نیز جذب روی را کاهش میدهد. قابلیت جذب روی به کی لات ساز در خاک که در اثر تراوش ریشه یا تجزیه مواد آلی تأمین میشود بستگی دارد.[4]
اهمیت روی بر افزایش کمی و کیفی محصولات کشاورزی
یکی از وظایف مهم روی در گیاهان ساخت پروتئین است، بنابراین کمبود روی موجب کاهش مقدار پروتئین و افزایش مقدار آمینواسیدهای آزاد و آمیدها میشود؛ و همچنین روی در تولید هورمون اکسین، آنزیمهای مسول تولید نشاسته، فتوسنتز، سوخت و ساز نیتروژن (فعال سازی آنزیم رداکتاز)، آنزیمهای انتقال دهنده فسفات (هگزوکیناز) و نیز در تولید تریپتوفان و هورمون رشد (اسید ایندول استیک) نقش مؤثری دارد. در حضور اسید ایندول استیک، کلروفیل بیشتری ساخته میشود، پیری به تأخیر افتاده و میزان فتوسنتز در نهایت افزایش مییابد[5]
وضعیت روی در خاک
روی در خاک بیشتر به صورت ترکیبات بسیار کم محلول هیدروکسید یا کربنات روی وجود داردکه بخش عمده آن به شکل غیرقابل استفاده برای گیاهان میباشند. روی برای گیاهان در اکثر خاکهای کشور کمتر از یک میلیگرم بر کیلوگرم تخمین زده میشود بنابراین گیاهان یا نمیتوانند ریزمغذیها را جذب کنند یا در صورت جذب به دلیل رسوب در آوندها، امکان استفاده از آنها وجود ندارد. تشابه الکترونی یون کادمیوم با یون روی موجب میشود که کادمیوم به جای روی جذب گیاه شود، لذا در خاکهایی که قابلیت استفاده از روی پایین است، جذب کادمیوم توسط ریشه گیاه افزایش مییابد.[6]
نشانهها ی کمبود روی


به صورت کوتولگی گیاه، کوچک ماندن برگها و کوتاه شدن میان گرهها، و با کاهش سبزینگی بین رگ برگها همراه است.[7]
کمبود روی در در خاکهای زراعی کشور به دلایل متعددی از جمله مصرف کودهای فسفاتی، بیشتر مشاهده میشود.
روش تولید فلز روی
برای تولید فلز روی ابتدا خاک معدنی روی خرد و آسیاب میشود و در صورت داشتن سرب به همراه خود، به واحد فلوتاسیون منتقل میشود تا سرب جدا شود. خاکهای سولفوره نیز پس از انتقال به کوره به حالت اکسیده تبدیل شده و قابل استفاده میشوند. پس از آمادهسازی خاک، کنسانترهٔ به دست آمده در مخازن استیل، توسط سولفوریک اسید و آب مورد عمل لیچینگ قرار میگیرند، سولفات آهن و سولفات آلومینیوم جهت رسوب دهی با هالوژنهایی نظیر کلر و فلوئور برای جلوگیری از چسبندگی در کاتدها استفاده میشوند. روی موجود در خاک با عمل لیپینگ حل شده و سولفات روی به دست میآید. نیکل، کبالت، کادمیوم، آهن و برخی عناصر دیگر موجود در خاک نیز به همراه روی حل میشوند، از این رو باید قبل از الکترولیز یونهای مزاحم حذف شوند. برای حذف آهن و کبالت از محلول، پرمنگنات پتاسیم به همراه آمونیوم پرسولفات اضافه میشود تا آهن دو ظرفیتی به آهن سه ظرفیتی تبدیل شود. با افزودن دوغاب آهک هیدراته به محلول و بالا بردن pH، آهن و کبالت اکسید شده و رسوب میدهند و از محلول جدا میشوند.[8]
نقش زیست شناختی
روی از عناصر ضروری زندگی انسان است که برای بقاء و زندگی وی لازم است. کمبود روی در حیوانات موجب افزایش وزن میشود. روی در انسولین Zinc Finger Proteins و آنزیمهایی مانند Super Oxide Dismutase وجود دارد. بر اساس بسیاری از منابع مصرف قرصهای حاوی روی میتواند در برابر سرما خوردگی و آنفلوانزا ایمنی ایجاد کند. با این حال هنوز بر سر این مسئله اختلاف نظر وجود دارد.
در واقع روی یک ماده معدنی اصلی کمیاب است که بعد از آهن، بیشترین میزان را در بدن داراست. روی بهطور عمده در ماهیچهها ذخیره میشود، اما در یاختههای خونی سفید و قرمز، پرده شبکیه چشم، استخوانها، پوست، کلیهها، کبد و پانکراس نیز یافت میشود. غده پروستات در مردان نسبت به سایر اعضا، بیشترین مقدار روی را داراست.
بعضی از تحقیقات و مطالعات نشاندهنده مؤثرترین قرصهای روی در جلوگیری و کاهش علایم سرماخوردگی بودهاست. شما میتوانید قرصهای روی را به راحتی از داروخانه برای درمان سرما خوردگی بخرید.
کاربردها در پزشکی
مکملهای روی میتوانند دارای این فواید باشند:
- کمک به جلوگیری از سرطان
- جلوگیری ودرمان ریزش مو
- تقویت فعالیت سیستم ایمنی
- تسریع بخشیدن به بهبود زخمها
- درمان آکنه
- جلوگیری از دژنراسیون ماکولا (از بین رفتن بینایی که در افراد مسن اتفاق میافتد)
- درمان بعضی از موارد بی اشتهایی عصبی (بی اشتهایی نشانهای از کمبود روی است و افراد در دهه دوم زندگی بیشتر در معرض خطر کمبود روی ناشی از فقر غذایی هستند).
- تقویت و بهبود باروری مردان مخصوصاً در بین سیگاریها.
- درمان روماتیسم مفصلی (با داشتن آثار ضد التهابی).
- درمان بیماری ویلسون (یک اختلال ناشی از ذخیره بیش از حد مس).
- کاهش تغییرات در حس چشایی طی درمان سرطان. یو
- تقویت حس چشایی و بویایی.
بعضی از بیماریها، بر روی جذب روی تأثیر میگذارند یا باعث افزایش نیاز به روی میشوند؛ لذا این بیماران از مکملهای روی سود میبرند:
- آکرو درماتیت آنتروپاتیکا (بیماری ارثی که به علت سوء جذب روی ایجاد میشود).
- الکلیسم
- دیابت قندی
- بیماری کلیه
- بیماری سلیاک
- بیماری روده التهابی مانند کولیت زخم شونده
- اسهال مزمن
- بیماریهای پانکراس
- مشکلات پروستات (بزرگی خوشخیم پروستات، تورم پروستات، سرطان پروستات) زنانی که حامله هستند یا بچه شیر میدهند یا اینکه از قرصهای خوراکی ضد حاملگی استفاده میکنند، نیز نیاز بیشتری به روی دارند.
منابع غذایی
ما ۲۰ تا ۴۰ درصد میزان روی موجود در غذا را جذب میکنیم. غذاهایی مانند گوشت قرمز، ماهی، مرغ و بوقلمون، آمادهترین شکل قابل دسترس روی قابل جذب هستند. روی موجود در سبزیجات کمتر برای بدن ما قابل دسترس است و فیبر سبزیجات به تنهایی میزان روی را که قابل جذب و استفاده است کمتر میکند. محصولات لبنی و تخم مرغ دارای میزان نسبتاً خوبی روی هستند اما جذب روی از این مواد مشکلتر است.

غذاهای زیر بهترین منبع قابل استفاده روی است:
صدف نرمتن (غنیترین منبع)، گوشت قرمز، میگو، خرچنگ و دیگر ماهیهای صدف، منابع دیگر روی که کمتر قابل جذب است شامل لوبیا، نخود چشم سیاه، سویا، بادام زمینی) غلات کامل، فیبرو، توفو، مخمر آبجو، سبزی پخته شده، قارچ، لوبیا سبز و دانه کدو است.
اشکال دیگر
سولفات روی رایجترین مکمل قابل استفاده روی است. این ترتیب نسبت به سایر اشکال کمترین قیمت را دارد. اما حداقل جذب را دارد و باعث آشفتگی معده میشود. پزشک معالج معمولاً ۲۲۰ میلیگرم از سولفات روی را که حاوی تقریباً ۵۵ میلیگرم عنصر روی است، تجویز میکند. شکلهای قابل جذب تر که قابل دسترس هستند عبارتاند از: پیکولینات روی، سیترات روی، استات روی، گیسرات روی و مونو میتونین.
اشکال مختلف روی دارای میزان متفاوتی از روی در ترکیب هستند. در برچسب این ترکیبات، همیشه به دنبال میزان عنصر روی بگردید. معمولاً ترکیبات روی دارای ۳۰ تا ۵۰ میلیگرم از عنصر روی هستند. به خاطر داشته باشید که از غذای روزانه چیزی حدود ۱۰ تا ۱۵ میلیگرم روی جذب میکنید، پزشک معالج شما هنگام تجویز مکملهای روی، باید این میزان دریافتی روزانه از طریق غذا را در نظر داشته باشد. قرصهای روی در داروخانهها قابل دسترس هستند و برای درمان سرماخوردگی مفید هستند. همچنین جوانه گندم منبع خوبی از روی میباشد که خوردن آن به همه افراد توصیه میشود.
نحوه مصرف
قبل از اینکه از مکملهای روی استفاده کنید یا پزشک متخصص تغذیه مشورت کنید. وقتی شما بهترین فایده را از مکملهای روی میبرید که آن را با آب یا آب میوه (نه با شیر) در بین غذاها مصرف کنید و همزمان با مکملهای آهن و کلسیم، آنها را مصرف نکنید. اگر برای معده شما مشکل ایجاد کرده باشد میتوانید آن را همراه غذا مصرف کنید.
موارد احتیاط
بیشتر مواد معدنی کمیاب، در صورت مصرف بیش از حد برای بدن سمی هستند و این نکته در مورد روی صدق میکند. نشانههای مسمومیت عبارتاند از: آشفتگی معده، و استفراغ و معمولاً وقتی ایجاد میشود که ۲۰۰۰ میلیگرم یا بیشتر مصرف شده باشد. مطالعات نشان میدهد که تا ۱۵۰ میلیگرم روی خطری ندارد اما معمولاً این میزان مورد نیاز نیست و با استفاده بدن از عناصر دیگر تداخل دارد. تحقیقات نشان میدهد که مصرف روزانه کمتر از ۵۰ میلیگرم مصرف مطمئنی است اما اطلاعاتی در مورد مصرف طولانی مدت این مقدار روی در دسترس نیست.
قبل از استفاده از روی یا سایر مکملها، با پزشک خود مشورت کنید.
یک عارضه جانبی منفی شناخته شده از روی این است که میزان زیاده روی باعث کاهش HDL (کلسترول خوب بدن) و افزایش LDL (کلسترول بد بدن) میشود. بعضی از تحقیقات نشان میدهد که مصرف خیلی زیاد روی باعث کاهش عملکرد ایمنی میشود در حالی که مطالعات دیگر این نظر را تأیید نمیکند. اگر سولفات روی باعث تحریک معده شود شکل دیگری از روی، برای مثال سیترات روی را مصرف کنید و قبل از آن با پزشک مشورت کنید. سایر عوارض جانبی از مسمومیت با روی عبارتاند از: سرگیجه، سردرد، خواب آلودگی، افزایش تعریق، ناهماهنگی عملکرد عضلات، عدم تحمل الکل، توهم و کم خونی.
تداخلهای احتمالی
چون روی با دیگر عناصر تداخل دارد شما میتوانید از مولتی ویتامین، یا عناصر خونی آماده شامل روی، آهن و فولات استفاده کنید. این به شما کمک میکند تا میزان عناصر را در یک حد تعادل نگه دارید. مصرف زیاد روی میتواند با جذب مس تداخل کرده و باعث کمبود مس شود. این مسئله به میزان آهن بدن اثر گذاشته و میتواند منجر به کم خونی شود.
مصرف زیاد آهن و مس با جذب روی تداخل میکند. روی با جذب فولات تداخل دارد. قبل از مصرف روی یا هر مکمل دیگر با پزشکتان مشورت کنید.
تداخلهای احتمالی عبارتاند از:
- ویتامین ب-۱۲ سطح تولید ملاتونین را تغییر میدهد. اگر سطح ملاتونین خون شما پایین میزان ویتامین ب-۱۲ نیز پایین است. مصرف ویتامین ب-۱۲ (۱/۵ میلیگرم متیل کوبالامین در روز) میتواند باعث بهبود اختلالات خواب شود، زیرا این ویتامین تولد ملاتونین را افزایش میدهد.
- داروهای ضد التهابی غیر استروییدی (NSAIDs)، مانند آسپیرین و ایبوپروفن سطح تولید ملاتونین در بدن را کاهش میدهد؛ بنابراین بهتر است قبل از خواب از این داروها استفاده نکنید. بتابلاکرها نیز مانع بالا رفتن ملاتونین در شب میشوند.
- پروتئین، ویتامین ب-۶، نیاسین آمید و استیل کارنیتین همگی به تولید ملاتونین کمک میکنند.
- بعضی از داروهای ضد افسردگی سطح ملاتونین مغز را افزایش میدهند. بنزودیازپینها، مانند والیوم و زاناکس (Xanax)، مانع از تولید ملاتونین میشوند.
الکل و کافئین و دیورتیک و بلوککنندههای کانال کلسیم مانع از تولید ملاتونین میشوند.
میزان مورد نیاز روزانه
بررسیهای انجام شده نشان میدهد که نیاز خانمها به این عنصر مهم وضروری روزانه، حداقل ۱۰ میلیگرم و نیاز آقایان روزانه، حداقل ۱۲ میلیگرم است. بیشتر دیده میشود که مقدار مصرفی روی بسیار کمتر از مقدار نیاز بررسی شدهاست.
مرکز تغذیه کشور آلمان (DGE) و آمریکا (RDA) توصیه میکنند که برای پیشگیری از امراض حاصل شده از کمبود روی، خانمها روزانه ۱۲ میلیگرم و آقایان ۱۵ میلیگرم روی به بدن خود برسانند. البته دوز و مقدار درمانی که توسط دکتر ورباخ بیان شده، روزانه بین ۱۰۰–۲۰ میلیگرم است. اصولاً” دوز ۱۵ میلیگرم در روز را حد متوسط دریافت روزانه میدانند.
دوز درمانی
دوز درمانی توسط روی روزانه حدوداً” ۵۰ میلیگرم است. تأمین روی به صورت ترکیبات گلوکونات روی برای بدن بسیار خوب و قابل تحمل و با جذب خوب است. به یاد داشته باشید که کلیه مکملهای حاوی روی بایستی همراه غذا مصرف شده تا از ایجاد تهوع جلوگیری شود(مصرف همزمان با مکمل آهن موجب کاهش جذب می شود). توجه داشته باشید، افرادی که به مدت طولانی روزانه ۵۰ تا ۳۰۰ میلیگرم روی مصرف کردهاند، میتوانند دچار اختلال جذب املاح آهن ومس شده و همچنین به کمبود این دو املاح در بدن دچار شوند. حتی دیده شدهاست کسانی که روزانه ۲ گرم به مدت طولانی روی خوردهاند، علائمی مثل استفراغ، تهوع، دردهای شکمی و تب را نشان دادهاند. افرادی که دچار ناراحتیهای کبد ی و رودهای اند، بایستی قبل از مصرف مکملهای حاوی روی، حتماً با پزشک خود مشورت داشته باشند.
روی و بیماریهای پوست
دیده شدهاست که غلظت روی در پوست و چشم بیشتر از هر عضو و اندامی در بدن است. مصرف روی در سوختگیها، اعمال جراحی وبهبود زخمهای بدن، ضروری است. روی باعث بهبود هر چه سریعتر زخمها میشود و کمبود روی بهبود زخمها را به تعویق میاندازد، به ویژه در بیماران دیابتی، زخمهای پا و عفونت این زخمها است که حتی میتواند به قطع عضو هم منجر شود.
بنابراین وجود روی به مقدار کافی در برنامه غذایی این افراد بسیار مهم است. مصرف روی در ترمیم سوختگیها، زیاد بوده و بهطور معمول در خون بیماران دچار سوختگی، کمبود روی مشاهده میشود و با دادن روی اضافی میتوان، بهبود و ترمیم زخم و پوست را تسریع کرد. این مسئله حتی در سوختگیهای درجه ۳ به دنبال مصرف محلولها و ترکیبات حاوی روی به اثبات رسیدهاست و هماکنون نیز از این ترکیبات (مانند پماد زینک اکساید و…) استفاده میشود.
به عبارتی روی به عنوان ترمیمکننده بافتی و پوستی شناخته شدهاست. افرادی که از اگزما و حساسیت زجر میبرند، بهطور معمول دارای سطح پایین روی در خون هستند و میتوان با دادن ۳۰ میلیگرم روی (معادل ۲۰۰ میلیگرم گلوکونات روی است) بهبود بیماری آنها را تسریع کرد.
روی و مرض قند
نکته دیگر در مورد مصرف روی و بیماران دیابتی این است که تأثیر انسولین بهطور مستقیم با روی در ارتباط است. میزان عنصر روی در پانکراس افراد سالم دو برابر دیابتیها است که میتواند نشانهٔ نقش آن در تولید انسولین باشد. مشاهده شدهاست که نقصان روی در خون باعث هیپو انسولینیمیا (کاهش انسولین خون) میشود. کمبود روی به صورت مزمن و دائمی صدمهٔ بزرگی به یاختههای بتا پانکراس که انسولین ترشح میکنند، میزند و در سنین بالا، افراد دارای کمبود طولانی مدت روی میتوانند دچار دیابت نوع ۲ بشوند.
بهطور کلی میتوان گفت که در خون اکثر افراد مبتلا به دیابت، کمبود روی دیده میشود و متأسفانه دفع روی در ادرار آنها مشاهده میشود؛ بنابراین رساندن روی اضافی به بدن بیماران دیابتی ضروری است.
فقر روی به ویژه در دیابتیها زخمهای مزمن ورید پا را ایجاد میکند که گاهی منجر به قطع انگشتان یا پا میشود. با دادن روی اضافی نه تنها زخمهای دیابتی زودتر ترمیم شده بلکه علاوه بر آن سطح سیستم ایمنی نیز افزایش مییابد.
عوارض کمبود روی در سایر موارد
به دنبال افت سیستم ایمنی در اثر کمبود روی، بیماریهای اتوایمیون (خودایمنی) مثل آرتریت روماتویید، لوپوس، شوگرن، پسوریازیس و… افزایش مییابد.
نقصان روی در مردان وزنان موجب اختلالات باروری میشود. اغلب مردان وزنان که جهت درمان مشکل خود اقدامات زیادی انجام دادهاند، باید مسئلهٔ کم بودن روی را نیز در نظر گرفته و نسبت به رفع آن اقدام کنند.
نقصان روی در بدن خانمهای باردار میتواند منجر به رشد ناکافی و کند جنین یا زایمان زودرس شود.
یکی از علل میوم رحم و کیستهای پستان در خانمها، کمبود روی میباشد و دیده شدهاست که با تجویز روی به بدن آنها بهبودی حاصل شدهاست. هم چنین دیده شدهاست که در خانمهایی که دچار عفونتهای راجعه قارچی دستگاه تناسلی میشوند و به هیچ درمان منظم دارویی جواب نمیدهند، تجویز روی به مقدار کافی، باعث بهبود آنها شدهاست.
هم چنین مصرف روی در بهبود ریزش مو به اثبات رسیدهاست و امروزه کمبود روی را از علل مهم ریزش مو میدانند، که البته بایستی سایر علل ریزش مو مانند کمبود ویتامینها، کم خونی و… نیز مد نظر قرار گیرد.
کمبود روی در کودکان همراه با بی اشتهایی، اختلال چشایی طعم غذا، پیکا (حالتی شبیه ویار حاملگی)، بیحالی، غش، اختلال رفتاری و وقفه در رشد، خود را نشان میدهد، هم چنین در نوجوانان به صورت تأخیر بلوغ جنسی و ظهور نکردن صفات ثانویه جنسی بروز میکند.
کمبود روی در افراد مسن، در هنگام راه رفتن، اختلال تعادل را ایجاد میکند که با تجویز داروی روی قابل درمان است.
روی در تشکیل هموگلوبین دخالت دارد و در مواردی فقط تجویز روی همراه دیگر نیازها، این عارضه را درمان میکند. روی در رشد فیزیکی بدن مؤثر است، هم چنین کوتاهی قد و کمبود وزن در کودکان ایرانی با تجویز روی قابل درمان است و بهتر میباشد که رساندن روی به مقدار کافی به بدن مادر در دوران بارداری و شیردهی مد نظر قرار گیرد. به علاوه باعث ریزش مو میشود.
جذب روی در بدن
جذب روی آسان نبوده و دفع آن نیز به سختی صورت میگیرد و به همین دلیل در تجویز روی و استفاده از آن باید رعایت این مشکل، منظور شود. به علت آن که روی در ناحیهٔ اولیهٔ روده باریک جذب میشود، پروتئین در جذب آن دخالت دارد و لازم است کمبود پروتئین در افراد دچار نقص روی نیز درمان شود.
پیدایش
روی بیست و سومین عنصر در پوسته زمین از نظر فراوانی میباشد. بسیاری از سنگهای معدنی سنگین استخراج شده حاوی ۱۰٪ آهن و ۴۰–۵۰٪ روی میباشند. معادنی که از آنها روی استخراج میشود شامل Sphakrite, Zinc Blende, Smith sonite, Calamine, Franklinite میشوند. تاکنون نزدیک به ۶۰ نوع کانی روی شناخته شدهاست روی عنصری بهطور طبیعی وجود ندارد. از این شمار سولفور روی با نام اسفالریت یا بلاند (ZnS) شناخته شده، مهمترین کانی است. از دیگر کانیهای با اهمیت روی میتوان به اسمیت زونیت ZnCO3، همی مورفیت (Zn4Si2O7(OH و زنسیت (ZnO) اشاره کرد.
ترکیبات
اکسید روی معروفترین ترکیبی است که بهطور گسترده در ترکیبات روی مورد استفاده قرار میگیرد و به عنوان رنگدانه سفید در رنگها استفاده میشود. همچنین در صنعت Rubber کاربرد داشته و به عنوان Opaque Sunscreen فروخته میشود. دیگر ترکیبات روی به استفاده غیر صنعتی میرسند مانند: کلرید روی در بو گیر سولفید روی در رنگهای شب تاب و متیل روی در آزمایشگاه شیمی آلی. تقریباً یک چهارم فراوردههای روی به صورت ترکیبات روی مورد مصرف قرار میگیرد.
ایزوتوپها
روی طبیعی در ۴ ایزوتوپ پایدار تشکیل شدهاست: Zn64 Zn-66, Zn-67, Zn-۶۸ که در این میان Zn۶۴ فراوانترین آنها (۴۸٫۶٪ فراوانی طبیعی) میباشد. برای این عنصر ۲۲ رادیو ایزوتوپ اکتیو شناسایی شدهاست که در میان آنها Zn-۶۵ با نیمه عمر ۲۴۴٫۲۶ روز و Zn-۷۲ با نیمه عمر ۴۶٫۵ ساعت پایدارترین و فراوانترین ایزوتوپ میباشند. دیگر ایزوتوپهای رادیو اکتیو این عنصر نیمه عمرهای کمتر از ۱۴ ساعت هستند و بیشتر آنها نیمه عمری کمتر از یک دقیقه دارند. این عنصر همچنین ۴ حالت متا دارد.
هشدارها
فلز روی سمی نیست اما حالتهایی به نام Zinc Shakes یا Zinc Chills وجود دارند که با استنشاق اکسید روی تازه و خالص تحریک میشوند.
شناخت محیط رشد روی
روی در تولید و فعالیت آنزیمها، همچنین در ایجاد پروتئین مؤثر است. کمبود روی باعث کوچک ماندن برگهای گیاه و کوتاه شدن فاصله میان گرهها میشود. واکنش خاک، بر قابل استفاده بودن روی برای گیاه، مؤثر میباشد. معمولاً در خاکهای قلیایی، و در خاکهای محتوی فسفر بیش از حد، روی غیرقابل استفاده میگردد. در خاکهای شنی، به راحتی شسته شده و از زمین خارج میشود. برای رفع کمبود روی، سولفات روی را به خاک اضافه میکنند. هر چند که شرایط خاکهای ایران سولفات روی شدیداً تثبیت میشود و بازده آن کم است و به صورت Zn EDTA بازده بیشتری دارد.
زینک یا روی یکی از مهم ترین عناصر اثر بخش در تولید تستوسترون طبیعی در بدن مردان است چرا که از تبدیل تستوسترون به استروژن (هورمون زنانه ) جلوگیری میکند ،با تولید انزیمی به نام ارومایتاس ازین عمل جلوگیری می کند .عکس عمل نیز در بدن توسط روی اتفاق می افتد یعنی هورمون های زنانه را به مردانه تبدیل میکند و باعث تولید اسپرم های سالم تر نیز می شود ،یعنی تبدیل استروژن به تستوسترون به صورت طبیعی ،منابع طبیعی برای جذب زینک یا روی در مواد غذایی : الف)جگر ب)غذاهای دریایی ج)حبوبات و دانه های روغنی د)تخم مرغ همچنین میزان مصرف صحیح روی را در تصویر زیر میتوانید مشاهده نمایید.
منابع
- Meija, J.; et al. (2016). "Atomic weights of the elements 2013 (IUPAC Technical Report)". شیمی محض و کاربردی(نشریه). 88 (3): 265–91. doi:10.1515/pac-2015-0305.
- منبع کتاب (نقش روی درافزایش کمی وکیفی محصولات کشاورزی وبهبودسلامتی جامعه) تألیف دکترملکوتی ودکترلطف اللهی
- «These Robots Can Store Energy in "Fat Reserves," Like Humans». futurism.
- جلیلی مرندی، رسول (۱۳۹۴). میوه کاری. ارومیه: جهاد دانشگاهی واحد آذربایجان غربی. صص. ۱۰۳. شابک ۹۷۸-۹۶۴-۶۰۳۲-۲۳-۱.
- ملکوتی، محمد جعفر (۱۳۹۴). توصیه بهینه مصرف کود برای مصرف محصولات کشاورزی در ایران. تهران: مبلغان. شابک ۹۷۸-۹۶۴-۲۶۱۴-۹۵-۰.
- ملکوتی، محمد جعفر (۱۳۹۴). توصیه بهینه مصرف کود برای محصولات کشاورزی ایران. تهران: مبلغان. شابک ۹۷۸-۹۶۴-۲۶۱۴-۹۵-۰.
- خوشخوی، مرتضی (۱۳۹۱). اصول نوین باغبانی. شیراز: دانشگاه شیراز. صص. ۱۷۶. شابک ۹۷۸-۹۶۴-۴۶۲-۴۵۴-۴.
| در ویکیانبار پروندههایی دربارهٔ روی موجود است. |

