کبد
جِگَر یا کَبِد (به انگلیسی: Liver) بزرگترین غده در بدن است[2] که در فعالیتهای سوختوساز بدن مانند گوارش و در سمزدایی نقش دارد.
| جگر | |
|---|---|
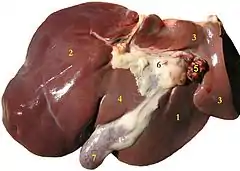 جگر گوسفند: (۱) لُبّ راست، (۲) لب چپ، (۳) لب دمی، (۴) لب چهارگوش، (۵) سرخرگ کبدی و سیاهرگ باب کبدی، (۶) گرههای لنفاوی کبدی، (۷) کیسه صفرا. | |
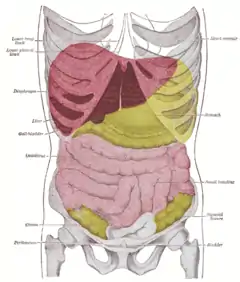 نمای قدامی از وضعیت کبد (قرمز) در شکم انسان. | |
| جزئیات | |
| ساخته از | پیشین روده |
| سیاهرگ | سیاهرگهای کبدی، ورید باب |
| عصب محیطی | گانگلیونهای سلیاک، عصب واگ[1] |
| شناسهها | |
| لاتین | jecur |
| MeSH | D008099 |
| TA98 | A05.8.01.001 |
| TA2 | 3023 |
| FMA | 7197 |
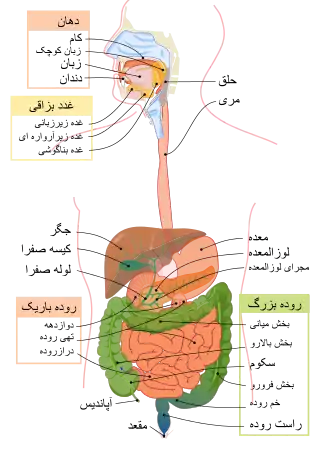
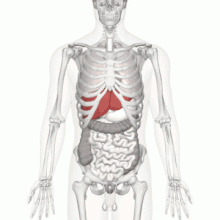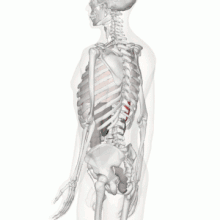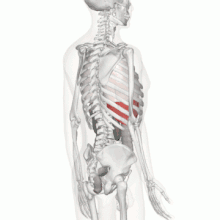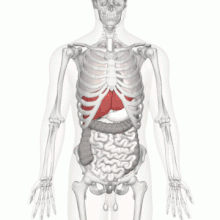
تمام خون دستگاه گوارش توسط سیاهرگ باب کبدی جمعآوری شده و وارد جگر میشود و تمام مواد جذب شده از لولهٔ گوارشی (بجز لیپیدها که بهصورت کیلو میکرون از طریق سامانه لنفی به بزرگ سیاهرگ زبرین میریزند) از جگر عبور میکنند. از دیگر کارهای جگر به دام انداختن سموم و تصفیهٔ آنها با تبدیل کردنشان به مواد بیضرر است. همچنین، این جگر است که سوخت و ساز (متابولیسم) داروها را در بدن بر عهده دارد. شرکت در خونسازی (در دورهٔ پیش از تولد) و مقاومت در برابر عفونتها، فراهم ساختن سریع انرژی در هنگام ضرورت، ذخیرهٔ آهن و… از دیگر فعالیتهای کبد است[3]
پروتئینهای خونی در جگر ساخته میشوند. سلولهای کبدی پروتئینهای مختلفی را بهطور دائمی میسازند از جمله آلبومین، پروترومبین، فیبرینوژن، لیپوپروتئینها و هپارین.[4]
سلولهای کبدی مواد مختلفی، از جمله تری گلیسریدها، گلیکوژن و ویتامینها را ذخیره میکنند.[4]
جگر به عنوان یک سیستم بافری مهم برای گلوکز خون عمل میکند به این معنی که هنگامی که گلوکز خون بعد از صرف یک وعده غذا تا غلظت زیادی بالا میرود میزان ترشح انسولین نیز افزایش مییابد و در حدود دو سوم گلوکز جذب شده از روده بلافاصله به گلیکوژن تبدیل شده و در جگر ذخیره میشود. در طی ساعتهای بعد که غلظت گلوکز خون، و نیز انسولین کاهش مییابد، جگر گلیکوژن را تجزیه و به گلوکز تبدیل میکند.
این تنظیم در بیماران با اختلالات کبدی تقریباً غیرممکن است.
کالبدشناسی
جگر عضو قهوهای مایل به قرمز با چهار لب نابرابر از نظر شکل و اندازه است. وزن طبیعی جگر انسان ۱٫۶۶–۱٫۴۴ کیلوگرم (۳٫۷–۳٫۲ پوند) بوده،[5] و اندامی صاف، صورتی-قهوهای و مثلثی شکل است. جگر بزرگترین اندام داخلی (پوست بزرگترین اندام کلی است) و بزرگترین غده در بدن انسان است. محل این اندام در یک چهارم بالایی حفره شکمی بوده، و درست زیر دیافراگم قرار دارد. جگر در سمت راست معده بوده و روی کیسه صفرا قرار دارد. دو رگ خونی به آن متصل شدهاست، یکی از آنها شریان کبدی و دیگری سیاهرگ باب نام دارد. شریان کبدی خون آئورتی را حمل میکند، در حالی که سیاهرگ باب خون شامل مواد مغذی هضم شده از گوارش و همچنین طحال و لوزالمعده را حمل میکند. این رگهای خونی به مویرگها تقسیم شده، و خون را به لبها هدایت میکنند. هر لب از میلیونها یاختهٔ کبدی تشکیل شده که اساس یاختههای متابولیکی هستند. لبها واحدهای عملکردی کبد هستند.
انواع سلول
دو نوع عمده از سلولهای عمومی در لبهای جگر وجود دارد؛ سلولهای نرماکنه (پارانشیم) و سختاکنه. ۸۰٪ حجم جگر را سلولهای نرماکنه تشکیل داده و هپاتوسیت نامیده میشوند. سلولهای سفتاکنه ۴۰٪ از تعداد کل سلولهای جگر را تشکیل میدهند اما تنها ۶٫۵٪ حجم جگر را شامل میشوند. سلولهای آندوتلیال سینوسی کبدی، سلولهای کوپفر و سلولهای ستارهای کبدی تعدادی از سلولهای سفتاکنه سینوس کبد هستند.[6]
جریان خون
جگر دارای جریان خون دوگانهای است: یکی از سیاهرگ باب٬ و دیگری از شریان کبدی. حدود ۷۵٪ از جریان خون جگر، توسط سیاهرگ باب از خون سیاهرگی طحال، دستگاه گوارش و اندامهای مرتبط با آن تأمین میشود. شریان کبدی باقیمانده جریان خون جگر را تأمین میکند. اکسیژن از هر دو منبع تأمین میشود؛ تقریباً نصف اکسیژن کبد توسط سیاهرگ باب و نصف آن توسط شریان کبدی تهیه میشود.[7]
خون در سینوسهای کبدی جریان یافته و داخل ورید مرکزی هر لب تخلیه میشود. وریدهای مرکزی با ورید کبدی که کبد را ترک میکند یکی میشوند.
جریان صفراوی
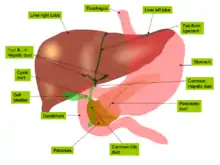
اصطلاح درخت صفراوی از شاخههای بلند مجاری صفراوی گرفته شدهاست. صفرای تولید شده در جگر در کانالهای صفراوی که با مجاری صفراوی ادغام شده، جمع میشوند. درون جگر، این مجاری، مجاری صفراوی داخل کبدی نامیده میشوند (درون کبد)، و هنگامی که خارج میشوند آنها را خارج کبدی (بیرون از کبد) مینامند. مجاری داخل کبدی در نهایت به مجاری کبدی چپ و راست تخلیه میشوند و با ادغام خود مجرای مشترک کبدی را میسازند. مجرای سیستیک کیسه صفرا با مجرای مشترک کبدی متصل شده و مجرای مشترک صفرا را تشکیل میدهند.
صفرا توسط مجرای مشترک صفرا مستقیماً وارد دوازدهه میشود، یا توسط مجرای سیستیک موقتاً در کیسه صفرا ذخیره میشود. مجرای مشترک صفرا و مجرای پانکراس با یکدیگر در آمپول واتر وارد بخش دوم دوازدهه میشوند.
جگر انسان
اگر سطح جداری را مشاهده کنید، جگر انسان بهطور معمول به دو لب تقسیم میشود (چپ و راست)؛ اما اگر سطح احشایی را مشاهده کنید کبد به چهار لب به علاوه لب دمی و چهارگوش تقسیم میشود. نشانههای کالبدشناسی دیگری نیز وجود دارد، از جمله لیگامان وریدی (لیگامان آرانشیو) و لیگامان دایرهای (لیگامان ترس) که بعداً در سمت چپ کبد به دو بخش تقسیم میشوند. لیگامان داسی (لیگامان فلسی فرم) در جلوی جگر (سمت قدامی) قابل مشاهده است. این لیگامان جگر را به دو لب چپ و راست تقسیم میکند.
بخشهای کالبدشناسی
جگر در طبقهبندی Couinaud کالبدشناسی کبد، به هشت بخش عملکردی مستقل تقسیم میشود (یا اگر بخشهای زیرین را حساب کنید به ۹ بخش تقسیم میشود).[8]
دیگر حیوانات
جگر در تمام مهرهداران وجود دارد، و بهطور معمول بزرگترین اندام (داخلی) است. شکل آن در گونههای مختلف متفاوت است، و به دلیل شکل بزرگش و ترتیب قرارگیری اندامهای اطراف آن قابل تشخیص است. با این حال، در بیشتر گونهها جگر به دو لب چپ و راست تقسیم میشود؛ استثنا در این قاعده کلی مارها هستند، که به دلیل ضرورت شکل بدن جگر آنها به شکل سیگار برگ وجود دارد. ساختار داخلی جگر آن کاملاً شبیه همه مهرهداران است.[9]
این اندام گاهی اوقات بهعنوان جگر مرتبط با دستگاه گوارش طنابداران اولیه مثل نیزک یافت میشود. هرچند، این اندام یک غده ترشحی است، نه یک اندام متابولیکی، و چگونگی همساختشناسی واقعی آن با کبد مهرهداران مشخص نیست.[9]
فیزیولوژی
عملکردهای مختلفی از جگر توسط سلولهای کبدی یا هپاتوسیتها انجام میشود. در حال حاضر، هیچ اندام مصنوعی یا دستگاهی که توانایی تقلید تمام عملکردهای جگر را داشته باشد وجود ندارد. در درمان تجربی نارسایی کبد بعضی از عملکردها را میتوان با دیالیز کبد مشابهسازی کرد. تصور میشود که جگر مسئول ۵۰۰ عملکرد جداگانه در ترکیب با دیگر سیستمها و اندامها است.
سنتز
- بخش بزرگی از سنتز اسیدآمینه
- جگر نقشهای متعددی در متابولیزم کربوهیدارتها دارد
- نوگلوکززایی (سنتز گلوکز از اسید آمینهها، لاکتات یا گلیسرول)
- گلیکوژنولیز (شکستن گلیکوژن به گلوکز)
- گلیکوژنز (تشکیل گلیکوژن از گلوکز)(بافتهای ماهیچهای نیز میتوانند این کار را انجام دهند)
- جگر مسئول اصلی متابولیزم پروتئینها، سنتز و همچنین تخریب آنها است.
- جگر چندین نقش متعدد در متابولیزم لیپیدها دارد:
- سنتز کلسترول
- لیپوژنزیس، تولیدات تریگلیسیریدها (چربیها)
- بخش عمدهای از لیپوپروتئینها در جگر سنتز میشوند.
- جگر فاکتورهای انعقادی I (فیبرینوژن)، II (پروترومبین)، V، VII، IX، X و XI، همچنین پروتئین سی، پروتئین اس و آنتیترومبین را تولید میکند.
- در سهماهه اول زندگی جنین، جگر اصلیترین محل برای تولید گلبول قرمز است. در هفته ۳۲ باروری، مغز استخوان تقریباً بهطور کامل این وظیفه را به عهده میگیرد.
- جگر صفرا (مایع زرد رنگ) را تولید و دفع میکند، صفرا برای امولسیون چربیها مورد نیاز بوده و بهجذب ویتامین کا کمک میکند. مقداری از صفرا مستقیماً وارد دوازدهه میشود و مقداری از آن در کیسه صفرا ذخیره میشود.
- جگر همچنین فاکتور رشد شبه انسولین ۱ را تولید میکند، هورمون پروتئینی پلیپپتیدی که نقش مهمی در رشد کودکان و تداوم آنابولیسم در بزرگسالان دارد.
- جگر محل عمده تولید ترومبوپپتین است. ترومبوپپتین یک هورمون گلیکوپروتئین است که تولید پلاکتها توسط مغز استخوان را تنظیم میکند.
تفکیک
سایر عملکردها
- جگر محل ذخیرهٔ بسیاری از مواد از جمله گلوکز (به شکل گلیکوژن)، ویتامین آ (ذخیره ۲–۱ سال)، ویتامین د (ذخیره ۴–۱ ماه)، ویتامین ب ۱۲ (ذخیره ۳–۱ سال)، ویتامین کا، آهن، و مس است.
- جگر مسئول اثرات ایمونولوژیکی است - سیستم فاگوسیتی تک هستهای (ام پی اس) جگر شامل بسیاری از سلولهای ایمونولوژیکی فعال است، همچنین به عنوان «غربال» برای آنتیژنهای حمل شده توسط سیستم باب عمل میکند.
- کبد، آلبومین، عمدهترین ماده اسمولاریته پلاسمای خون را تولید میکند.
- جگر آنژینوتانسینوژن را سنتز میکند، هورمون مسئول بالا بردن فشار خون، که توسط رنین فعال میشود، زمانی که کلیه احساس کند فشار خون پایین است رنین را آزاد میکند.
- جگر بهعنوان مخزن خون نیز عمل میکند، یک اندام قابل بسط است. مقدار زیادی از خون میتواند در رگهای خونی ذخیره شود، این مقدار حجم نرمال خون در وریدهای کبدی است و در سینوسهای کبدی در حدود ۴۵۰ میلی لیتر است. در طول نارسایی قلبی با احتقان محیطی، جگر گسترش مییابد، و گاهی اوقات ۰٫۵ تا ۱ لیتر از خون اضافی به علت فشار بالا در دهلیز راست که باعث بازگشت فشار در کبد میشود در وریدهای کبدی و سینوسها ذخیره میشود.
ارتباط با پزشکی و داروشناسی
ظرفیت اکسیداتیو جگر با افزایش سن کاهش مییابد بنابراین هر دارویی که به اکسیداسیون نیاز داشته باشد (مثلاً بنزودیازپین) احتمال زیاد دارد که به سطوح سمیت برسد. هرچند، داروهایی با نیمهعمر کوتاه، از جمله لورازپام و زازپام در بیشتر مواردی که بنزودیازپین در طب سالمندان مورد نیاز است، ترجیح داده میشوند.
بیماریهای جگر
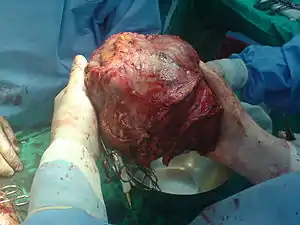
جگر تقریباً از هر اندامی در بدن حمایت میکند و برای بقا حیاتی است. بهدلیل محل استراتژیک و عملکردهای چندبعدی خود جگر نیز مستعد بسیاری از بیماریها است.[11]
عمومیترین بیماریها شامل: عفونتهایی از جمله هپاتیتهای آ، ب، سی، دی، ای، آسیبهای ناشی از نوشیدنیهای الکلی، کبد چرب، سیروز، سرطان، آسیبهای دارویی (به خصوص توسط استامینوفن (پاراستامول) و داروهای ضد سرطانی).
بسیاری از بیماریهای کبدی با یرقان ناشی از افزایش سطح بیلیروبین در سیستم همراه است. بیلیروبین نتیجه فروپاشی هموگلوبین گلبولهای قرمز خون است؛ بهطور معمول، جگر بیلی روبین را از خون خارج کرده و از طریق صفرا دفع میکند.
بسیاری از بیماریهای کبدی در کودکان نیز وجود دارد، از جمله انسداد مجاری صفراوی، کمبود آلفا-۱ آنتیتریپسین، سندرم آلاژیل، کلستاز داخل کبدی خانوادگی پیشرونده و هیستوسیتوز سلول لانگرهانس.
بیماریهایی که با عملکرد جگر تداخل دارند اختلالاتی را در فرایندهای آن ایجاد خواهند کرد. هرچند، جگر ظرفیت بالایی برای بازسازی و ذخیرهسازی دارد. در بیشتر موارد، جگر تنها علائم را بعد از آسیب گسترده نشان میدهد.
بیماریهای جگر با آزمون عملکرد کبد تشخیص داده میشوند، بهعنوان مثال، توسط تولید پروتئین فاز حاد.
همچنین بیماریهای دیگری نیز هستند که بهطور مستقیم بیماری جگر شناخته نمیشوند ولی ممکن است موجب اختلال در عملکرد جگر شوند، به عنوان مثال عامل دیفتری در گلو رشد میکند و توکسین آن بر جگر و کلیه و اعصاب و قلب اثر میکند. همچنین یکی از علل مرگ بیماری مالاریا نارسایی جگر و کلیه است.
بازسازی و پیوند
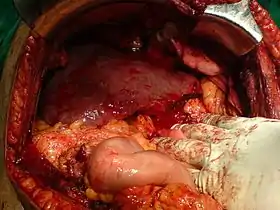
جگر تنها اندام داخلی بدن انسان است که توانایی باززایی طبیعی بافتهای از دست رفته را دارد؛ کمتر از ۲۵٪ جگر میتواند بهتمام جگر احیا شود.[12] باززایی بسیار سریع است. جگر طی یک تا دو هفته بعد از از دست دادن بیش از ۵۰٪ حجم خود به اندازه طبیعی خود باز خواهد گشت.
این عمل دلیل عمدهٔ بازگشت هپاتوسیتها به چرخه یاختهای است. هپاتوسیتها از فاز جی صفر خاموش به فاز جی ۱ رفته و تحت میتوز قرار میگیرند. این فرایند توسط گیرنده پی ۷۵ فعال میشود.[13]
سه پیوند اولیهٔ جگر انسان توسط توماس استارزل در سال ۱۹۶۳ در ایالات متحده انجام شد.[14] در سال ۱۹۶۸، روی کالن در کمبریج انگلستان اولین پیوند جگر را در بریتانیای کبیر انجام داد.[15]
پیوند کبد تنها گزینه برای افرادی است که مبتلا به نارسایی غیرقابل بازگشت کبدی هستند. بیشتر پیوندهای انجام شده برای بیماریهای مزمن باعث سیروز میشوند، از جمله هپاتیت سی مزمن، الکلیسم، هپاتیتهای خودایمن و بسیاری دیگر از بیماریها. پیوندهای جگر انجام شده برای نارسایی حاد کبد که در آن نارسایی در طول چند روز هفته رخ میدهد کمتر شایع است.
پیشرفت
اندامزایی
منشأ جگر قرارگیری آن در بخش شکمی اندوردم فورگات (اندودرم یکی از ۳ لایه سلولی جوانه جنینی است) و مجاور مزانشیم دیواره ترنسورسوم است. در رویان انسان، دایورتیکولوم کبد یک لوله اندودرمی است که از فورگات به اطراف مزانشیم گسترش یافتهاست. مزانشیم دیواره ترانسورسوم باعث تکثیر این اندودرم به شاخه شاخه شدن و شکلگیری اپیتلیوم غدهای جگر میشود. بخشی از دایورتیکولوم کبدی (که این منطقه نزدیک لوله گوارش است) در ادامه به عنوان مجرای زهکشی جگر عمل میکند، و شاخهای از این مجرا کیسه صفرا را ایجاد میکند.[17] علاوه بر این سیگنالهای مزانشیم دیواره ترانسورسوم، فاکتور رشد فیبروبلاست از تکامل قلب نیز همراه با رتینوئیک اسید ناشی از مزودرم صفحه جانبی به صلاحیت جگر کمک میکند. سلولهای اندودرمی کبدی تحت یک انتقال مورفولوژیکی از ستونی به شبه لایهای منجر به ضخامت اولیه جوانه جگر میشود. سلولهای ستارهای جگر از مزانشیم مشتق میشوند.[18]
بعد از مهاجرت هپاتوبلاستها به مزانشیم دیواره ترانسورسوم، معماری کبدی با سینوسهای کبدی شروع بهکار میکند و مویرگهای صفراوی ظاهر میشوند. جوانهٔ جگر به لبهای کبدی تقسیم میشود. ورید نافی چپ به مجراهای وریدی تبدیل شده و ورید ویتلاین به ورید باب تبدیل میشود. گسترش جوانهٔ جگر توسط سلولهای بنیادی خونساز انجام میشود. هپاتوبلاستهای دو پتانسیلی به سلولهای اپیتلیال صفراوی و هپاتوسیتها متمایز میشوند. سلولهای اپیتلیال صفراوی از هپاتوسیتهای اطراف ورید باب متمایز میشوند، ابتدا یک، تکلایه تولید و سپس دولایه از سلولهای مکعبی تولید میکنند. در صفحهٔ داکتال، تمرکز انبساط در نقاطی از دولایه پدیدار میشود، توسط مزانشیم باب محصور شده، و تحت توبولزایی در مجراهای صفراوی درون کبدی قرار میگیرد. هپاتوبلاستها مجاور ورید باب قرار نگرفته و در عوض به هپاتوسیتها متمایز شده و در طنابهای خطی سلولهای اپی تلیال مزانشیم و مجراهای صفرا قرار میگیرند. هنگامی که هپاتوبلاستها به هپاتوسیتها تخصصی شده و گسترش مییابند، عملکردها را از یک هپاتوسیت بالغ دریافت میکنند، و در نهایت هپاتوسیتهای بالغ بهعنوان سلولهای اپیتلیال بسیار قطبی با انباشتگی گلیکوژن فراوان ظاهر میشوند.
تأمین خون جنین
در جنین در حال رشد، منبع اصلی خون کبد از ورید نافی است که مواد مغذی را برای جنین در حال رشد تأمین میکند. ورید نافی از ناف وارد شکم میشود، و در طول لبه آزاد لیگامان فلسی فرم کبد به سطح تحتانی کبد به طرف بالا عبور میکند. به شاخه چپی ورید باب متصل میشود. مجراهای وریدی، خون را از ورید باب چپی به ورید کبدی چپی و سپس به بزرگسیاهرگ زیرین حمل میکنند، و اجازه میدهند خون جنینی در کبد دور بزند.
درجنین، کبد در طول بارداری نرمال توسعه مییابد، و تصفیه نرمال کبد جنین انجام نمیشود. کبد اجازه ندارد فرایندهای گوارشی را انجام دهد زیرا جنین وعدههای غذایی را بهطور مستقیم مصرف نمیکند، اما مواد مغذی را توسط جفت از مادر دریافت میکند. کبد جنین برخی از سلولهای بنیادی خون را آزاد میکند که به تیموس جنین مهاجرت میکنند، بنابراین ابتدا لنفوسیتها، که لنفوسیت تی نامیده میشوند از سلولهای بنیادی کبد جنین ساخته میشوند. هنگامی که جنین متولد میشود، تشکیل سلولهای بنیادی خون در جنین به مغز قرمز استخوان منتقل میشود.
بعد از تولد، ورید نافی و مجراهای وریدی طی دو تا پنج روز کاملاً محو میشوند.
به عنوان غذا
جگر پستانداران، غازماکیانسانان، و ماهی معمولاً به عنوان خوراک توسط انسانها خورده میشود. جگرهای گاو، گوسفند، گوساله، مرغ خانگی و غازها در قصابیها و سوپرمارکتها بهطور گسترده قابل دسترس هستند.
جگر میتواند پخته، آبپز، کبابی، سرخ شده، در روغن تفت داده شده یا خام خورده شود (asbeh nayeh or sawda naye در غذاهای لبنانی، و همچنینساشیمی کبد در ژاپن). در بسیاری از آمادهسازیها، تکههای جگر با تکههای گوشت و کلیه، مانند اشکال مختلف کبابهای شبکهای خاورمیانهای ترکیب میشوند (به عنوان مثال meurav Yerushalmi). جگر اغلب در پخشینه درست میشود. مثالهای خوب شناخته شده شامل liver pâté، جگر چرب، chopped liver، و leverpastej میباشند. سوسیسهای کبدی از جمله Braunschweiger و liverwurst نیز ارزش غذایی دارند. خوراک سنتی آفریقای جنوبی، به نام Skilpadjies، از جگر گوسفند چرخ شده پیچیده در netvet (چربی غشا پوششی) تهیه شده و روی آتش کباب شدهاست. البته این نوع کباب جگر درایران در میان اقوام لر نیز مرسوم است ولی آن را چرخ نمیکنند بلکه به صورت قطعات کوچک در چربی غشا روده قرار میدهند.
جگر حیوانات غنی از آهن و ویتامین آ میباشند، و روغن جگر ماهی معمولاً به عنوان مکمل غذایی استفاده میشود. بهطور سنتی، کبد بعضی از ماهیها مخصوصاً لقمهماهی معمولی بهعنوان غذا ارزش دارد. این جگر برای آمادهسازی غذا مورد استفاده قرار میگیرد، از جمله در جگر اسکیت آبپز با تست در انگلستان، همچنین beignets de foie de raie و foie de raie en croute در آشپزی فرانسوی.[19]
خوردن جگر در دوران بارداری
اگرچه جگر به دلیل داشتن مواد مغذی و ویتامینهای متعدد مانند اسیدفولیک، پروتئین، ویتامین آ و آهن غذای بسیار مفیدی برای زنان باردار محسوب میشود. اما باتوجه به مقادیر زیاد ویتامین آ موجود در آن میتواند مشکلات متعدد و جدی برای جنین و مادر بهوجود آورد. ویتامین آ موجود در جگر به شکل رتینول است، رتینول بهطور قابل توجهی قویتر از خود ویتامین آ است که در صورت مصرف آن در مقادیر زیاد در دوران بارداری در رشد جنین و نواقص احتمالی و ایجاد سرطان در بدن مادر تأثیر دارد؛ لذا خوردن جگر در دوران بارداری باید با مشورت پزشک انجام شود.[20]
اشارات فرهنگی
در استورههای یونانی، پرومته بهدلیل آشکار کردن آتش برای انسان توسط خدایان مجازات شد، او را در جایی که یک کرکس (یا یک عقاب) جگر او را نوک میزد به سنگ زنجیر کردند و جگر در طول شب دوباره ساخته میشد. (جگر تنها اندام داخلی انسان است که میتواند خودش را به میزان قابل توجهی بازسازی کند) بسیاری از مردم باستانی خاور نزدیک و مناطق مدیترانهای نوعی از طالعبینی به نام هاروسپیسی را انجام میدهند، آنها سعی میکنند اطلاعات را با تمرین بر روی جگرهای گوسفند و دیگر حیوانات بهدست بیاورند.
در افلاطون، و در فیزیولوژیهای بعدی، جگر بهعنوان مکان تاریکترین احساسات تصور میشود (بهطور خاص خشم، حسادت و طمع) که انسان را به واکنش وادار میکند.[21] در تلمود (رساله براکهوت ۶۱ ب) کبد به عنوان محل خشم است که با کیسه صفرا خنثی میشود.
در زبانهای فارسی، اردو و هندی (جگر یا जिगर یا jigar) در سخنرانیهای تمثیلی جگر، مرجع شجاعت و احساسات قوی یا «بهترین حالت فرد» است.
افسانه جانسون کبدخوار میگوید که او میتواند جگر هرکسی را که بعد از شام کشته شده باشد، بریده و بخورد.
در فیلم رسالت، خوردن جگر حمزه بن عبدالمطلب در طول غزوه احد توسط هند دختر عتبه به تصویر کشیده شدهاست. اگرچه روایاتی وجود دارد که هند به جای خوردن جگر حمزه «طعم آن را چشید»، صحت این روایات جای سؤال دارد.
منابع
| در ویکیانبار پروندههایی دربارهٔ کبد موجود است. |
- Physiology at MCG 6/6ch2/s6ch2_30
- حسنزاده طاهری، محمد مهدی. ابرهیم زاده بیدسکان، علیرضا (۱۳۸۷)، آناتومی انسانی پایه، جهاد دانشگاهی مشهد، شابک ۹۶۴۳۲۴۱۸۱۵ از پارامتر ناشناخته
|نوبت چاپ=صرفنظر شد (کمک) - «کبد (1)». بایگانیشده از اصلی در ۱۴ مه ۲۰۱۱. دریافتشده در ۵ آوریل ۲۰۱۱.
- : کبد
- Cotran, Ramzi S. ; Kumar, Vinay; Fausto, Nelson; Nelso Fausto; Robbins, Stanley L. ; Abbas, Abul K. (2005). Robbins and Cotran pathologic basis of disease (7th ed.). St. Louis, MO: Elsevier Saunders. p. 878. ISBN 0-7216-0187-1.
- Kmieć Z (2001). "Cooperation of liver cells in health and disease". Adv Anat Embryol Cell Biol. 161: III–XIII, 1–151. PMID 11729749.
- Shneider, Benjamin L. ; Sherman, Philip M. (2008). Pediatric Gastrointestinal Disease. Connecticut: PMPH-USA. p. 751. ISBN 1-55009-364-9.
- Smithuis, Robin. "Anatomy of the liver segments". Radiology Assistant. Retrieved 9 February 2014.
- Romer, Alfred Sherwood; Parsons, Thomas S. (1977). The Vertebrate Body. Philadelphia, PA: Holt-Saunders International. pp. 354–5. ISBN 0-03-910284-X.
- «بیماریهای کبد». بایگانیشده از اصلی در ۵ مه ۲۰۱۱. دریافتشده در ۵ آوریل ۲۰۱۱.
- Cirrhosis Overview بایگانیشده در ۳۰ اکتبر ۲۰۱۱ توسط Wayback Machine National Digestive Diseases Information Clearinghouse. Retrieved on 2010-01-22
- Dieter Häussinger, ed. (2011). Liver Regeneration. Berlin: De Gruyter. p. 1. ISBN 978-3-11-025079-4.
- Suzuki K, Tanaka M, Watanabe N, Saito S, Nonaka H, Miyajima A (2008). "p75 Neurotrophin receptor is a marker for precursors of stellate cells and portal fibroblasts in mouse fetal liver". Gastroenterology. 135 (1): 270–281.e3. doi:10.1053/j.gastro.2008.03.075. PMID 18515089.
- Starzl, T.E. , T.L. Marchioro, K.N. Von Kaulla, G. Hermann, R.S. Brittain, W.R. Waddell, "Homotransplantation of the liver in humans." Surg Gynecol Obstet 117: 659-676, 1963.
- R.Y. Calne, R. Williams, "Liver transplantation in man. I. Observations on technique and organization in five cases." Br Med 4: 535-540, 1968.
- «تازهترین نتایج ۲۵ سال «پیوند کبد» ایران». خبرگذاری مهر.
- Gilbert SF (2000). Developmental Biology (6th ed.). Sunderland (MA): Sinauer Associates.
- Berg T, DeLanghe S, Al Alam D, Utley S, Estrada J, Wang KS (2010). "β-catenin regulates mesenchymal progenitor cell differentiation during hepatogenesis". J Surg Res. 164 (2): 276–85. doi:10.1016/j.jss.2009.10.033. PMC 2904820. PMID 20381814.
- Calvin W. Schwabe Unmentionable Cuisine (انگلیسی)
- خوردن جگر در بارداری
- Krishna, Gopi (1970). Kundalini – the evolutionary energy in man. London: Stuart & Watkins. p. 77. SBN 7224 0115 9. Unknown parameter
|coauthors=ignored (|author=suggested) (help)
