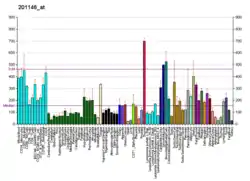
NFE2L2
فاکتور شبه هستهای ۲ مشتق از اریتروئید ۲ (انگلیسی: Nuclear factor (erythroid-derived 2)-like 2) که به اختصار «NFE2L2» یا «Nrf2» گفته میشود، یک فاکتور رونویسی است که در انسان توسط ژن «NFE2L2» کدگذاری میشود.[4] این ملکول، یک پروتئین دارای دومین بیزیپ است که بیانِ ژنهای مسئولِ تولید پروتئینهای آنتیاکسیدان را تنظیم میکنند. این پروتئینهای آنتیاکسیدان کارشان آن است که از تخریب اکسیداتیو سلولی در اثر التهاب یا صدمه به آنان جلوگیری کنند.
این پروتئین در مقادیر زیاد در کلیهها، ماهیچهها، ریه، قلب، کبد و مغز (به ترتیب میزان غلطت) تولید میشود.[4]
بیان پروتئین های آنتی اکسیدانی را که حفاظت در برابر آسیب استرس اکسیداتیو را به عهده دارند در اثر آسیب و التهاب تنظیم می کند. داروهای متعددی که مسیر NFE2L2 را تحریک می کنند ، برای درمان بیماری هایی که ناشی از استرس اکسیداتیو هستند ، مورد مطالعه قرار گرفته اند.
در شرایط عادی NRF2 در سیتوپلاسم به دام افتاده است و به منظور تجزیه ی پروتئوزومی در تعامل با پروتئین 1 مرتبط با ای سی اچ ((kelch-like ECH-associated protein1(Keap1) قرار دارد. در حضور گونه های فعال اکسیژن، سیستئین های کلیدی در ساختار Keap1 اکسید شده، منجر به تغییر کنفورماسیون و رهایش NRF2 می شوند. NRF2 به هسته منتقل شده و رونویسی از ژن های هدف را سبب می شود.
تقریباً در 20% از سرطان های ریه KRAS-driven non-small-cell (NSCLC) که یکی از تهاجمی ترین زیر گروه های سرطان ریه است، Keap1 یا NRF2 دچار جهش شده است. مطالعات Sarah E.LeBoeuf و همکاران نشان داده است که تومورهای جهش یافته Keap1/NRF2 برای حفظ تکثیر وابسته به تأمین گلوتامین خارجی هستند.
طی مطالعات Sarah E.LeBoeuf و همکاران نشان داده شد که جهش در Keap1 وابستگی به جذب خارجی چندین نوع اسید آمینه غیر ضروری در رده های Kras-driven ایجاد می کند. جذب اسید امینه های غیر ضروری در این سلول ها افزایش یافته و نسبت به محرومیت آسپارژین، گلایسین و سرین در شرایط درون تنی و برون تنی حساس هستند. مسدودسازی جریان خروج گلوتامات و در نتیجه افزایش سطح گلوتامات داخل سلولی از طریق مهار سیستم سیستئین/گلوتامات برای نجات سنتز اسیدآمینه و تکثیر سلولی در شرایط محرومیت اسید آمینه غیر ضروری کافی است. نشان داده شد که با محدودیت دارویی یا وابسته به NRF2 گلوتامات داخل سلولی می توان رشد تومور را با محدود سازی رژیم غذایی یا حذف آنزیمی اسیدآمینه های غیر ضروری در داخل بدن سرکوب کرد.[5]
منابع
- GRCm38: Ensembl release 89: ENSMUSG00000015839 - Ensembl, May 2017
- "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- Moi P, Chan K, Asunis I, Cao A, Kan YW (Oct 1994). "Isolation of NF-E2-related factor 2 (Nrf2), a NF-E2-like basic leucine zipper transcriptional activator that binds to the tandem NF-E2/AP1 repeat of the beta-globin locus control region". Proceedings of the National Academy of Sciences of the United States of America. 91 (21): 9926–30. doi:10.1073/pnas.91.21.9926. PMC 44930. PMID 7937919.
- LeBoeuf SE, Wu WL, Karakousi TR, Karadal B, Jackson SR, Davidson SM, Wong KK, Koralov SB, Sayin VI, Papagiannakopoulos T. Activation of Oxidative Stress Response in Cancer Generates a Druggable Dependency on Exogenous Non-essential Amino Acids. Cell Metabolism. 2019 Dec 5.
- مشارکتکنندگان ویکیپدیا. «NFE2L2». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۱۸ مارس ۲۰۱۸.
پیوند به بیرون
- NFE2L2 protein, human در سرعنوانهای موضوعی پزشکی (MeSH) در کتابخانهٔ ملی پزشکی ایالات متحدهٔ آمریکا