کالیفرنیوم
کالیفرنیوم یک عنصر شیمیایی رادیواکتیو با نماد Cf و عدد اتمی ۹۸ است. این عنصر برای اولین بار در سال ۱۹۵۰ در آزمایشگاه ملی لارنس برکلی (سپس آزمایشگاه پرتو دانشگاه کالیفرنیا) با بمباران کوریوم با ذرات آلفا (یونهای هلیوم-۴) ساخته شد. این عنصر یک اکتینید است، ششمین عنصر فرااورانیم است که باید سنتز شود و دارای دومین جرم اتمی پس از اینشتینیم در بین تمام عناصر تولید شده در مقادیر کافی برای دیدن با چشم غیرمسلح است. این عنصر به نام دانشگاه و ایالت کالیفرنیا نامگذاری شد.
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| کالیفرنیوم | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| تلفظ | /ˌkælɪˈfɔːrniəm/ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ظاهر | نقرهای | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد جرمی | ۲۵۱ (پایدارترین ایزوتوپ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| کالیفرنیوم در جدول تناوبی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اتمی (Z) | 98 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| گروه | بلوک جدول تناوبی | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دوره | دوره 7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| بلوک | بلوک-f | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دسته | Actinide | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| آرایش الکترونی | [Rn] 5f10 7s2[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| لایه الکترونی | 2, 8, 18, 32, 28, 8, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای فیزیکی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| فاز در STP | solid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه ذوب | 1173 کلوین (900 سانتیگراد )[2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه جوش | 1743 کلوین (1470 سانتیگراد ) (estimation)[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| چگالی (نزدیک r.t.) | 15.1 گرم بر سانتیمتر مکعب[2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای اتمی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اکسایش | +2, +3, +4, +5[4][5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الکترونگاتیوی | مقیاس پائولینگ: 1.3[6] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| انرژی یونش |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Color lines in a spectral range | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دیگر ویژگیها | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ساختار بلوری | شبکه کریستالی هگزاگونال فشرده (dhcp)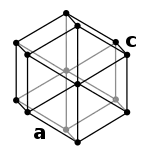 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سختی موس | 3–4[8] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شماره ثبت سیایاس | 7440-71-3[2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| تاریخچه | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نام | after California, where it was discovered | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| کشف | Lawrence Berkeley National Laboratory (1950) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ایزوتوپهای اصلی کالیفرنیوم[9][10] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
دو ساختار بلوری برای کالیفرنیوم تحت فشار عادی وجود دارد: یکی بالاتر و دیگری زیر ۹۰۰ درجه سلسیوس (۱٬۶۵۰ درجه فارنهایت) شکل سوم با فشار زیاد حاصل میشود. کالیفرنیوم به آرامی در دمای اتاق هوا کدر میشود. ترکیبات کالیفرنیوم در سطح اکسیداسیون +۳ موجود است. بیست ایزوتوپ کالیفرنیوم شناخته شدهاست، که کالیفرنیوم -۲۵۱ پایدارترین آنهاست که دارای نیمه عمر ۸۹۸ سال است. این نیمه عمر کوتاه به معنی این است که این عنصر در مقادیر قابل توجهی در پوسته زمین یافت نمیشود. [persian-alpha 1] کالیفرنیوم -۲۵۲، با نیمه عمر حدود ۲٫۶۴۵ سال، رایجترین ایزوتوپ مورد استفاده است و در آزمایشگاه ملی اوک ریج در ایالات متحده و پژوهشگاه رآکتورهای اتمی در روسیه تولید میشود.
کالیفرنیوم یکی از معدود عناصر فرااورانیم است که کاربردهای عملی دارد. بیشتر این کاربردها از خاصیت ایزوتوپهای خاص این عنصر برای انتشار نوترونها استفاده میکنند. به عنوان مثال، کالیفرنیوم میتواند برای کمک به راه اندازی راکتورهای هسته ای مورد استفاده قرار گیرد، و هنگام مطالعه مواد با استفاده از پراش نوترون و طیفسنجی نوترون به عنوان منبع نوترون استفاده میشود. کالیفرنیوم همچنین میتواند در سنتز هسته ای عناصر دارای جرم بالاتر مورد استفاده قرار گیرد. اوگانسون (با عدد اتمی ۱۱۸) با بمباران اتمهای کالیفرنیوم-۲۴۹ با یونهای کلسیم-۴۸ سنتز شد. استفادهکنندگان کالیفرنیوم باید نگرانیهای رادیولوژی و توانایی این عنصر را در ایجاد اختلال در تشکیل گلبولهای قرمز با تجمع بیولوژیکی در بافت اسکلتی در نظر بگیرند.
تاریخچه
کالیفرنیوم برای اولین بار در آزمایشگاه تابش دانشگاه کالیفرنیا در برکلی، توسط محققان فیزیک استنلی جی تامپسون ، کنت استریت جونیور، آلبرت غیورسو و گلن تی سیبورگ در تاریخ ۹ فوریه سال ۱۹۵۰ ساخته شد.[11] این ششمین عنصر ترانس اورانیوم بود که کشف شد. این تیم کشف خود را در ۱۷ مارس ۱۹۵۰ اعلام کرد.[12][13]
برای تولید کالیفرنیوم، یک هدف به اندازه میکروگرم از کوریوم -۲۴۲ (242
96Cm) با ۳۵ ذره MeV-alpha (4
2He) بمباران شد در سیکلوترون با قطر ۶۰ اینچ (۱٫۵۲ متر) در برکلی، که کالیفرنیوم ۲۴5 (۲۴۵
98Cf) به علاوه یک نوترون آزاد تولید کرد.[14][12]
- 242
96Cm + 4
2He → 245
98Cf + 1
0n
برای شناسایی و جداسازی عنصر، روشهای تبادل یونی و جذب استفاده شد.[15][12] در این آزمایش فقط حدود ۵۰۰۰ اتم کالیفرنیوم تولید شد[16] و این اتمها نیمه عمر ۴۴ دقیقه داشتند.[11]
ویژگیها
کالیفرنیوم در حقیقت یک فلز آکتینید نقرهای مایل به سفید[17] با نقطه ذوب ۹۰۰ ± ۳۰ درجه سلسیوس (۱٬۶۵۰ ± ۵۰ درجه فارنهایت) و نقطه جوش ۱٬۷۴۵ کلوین (۱٬۴۷۰ درجه سلسیوس؛ ۲٬۶۸۰ درجه فارنهایت) میباشد.[18] فلز ناب و خالص کالیفرنیوم قابلانعطاف است و به سادگی با تیغ بریده میشود. این فلز در خارج از محیط نگهداری و ایزوله و با دمای بالای ۳۰۰ درجه سلسیوس (۵۷۰ درجه فارنهایت) شروع به تبخیر مینماید.[19] در دمای ۵۱ کلوین (−۲۲۲ درجه سلسیوس؛ −۳۶۸ درجه فارنهایت) فرومغناطیس و فریمغناطیس است (چیزی شبیه به آهنربا). در دمای ۴۸ کلوین (−۲۲۵ درجه سلسیوس؛ −۳۷۳ درجه فارنهایت) تا ۶۶ کلوین (−۲۰۷ درجه سلسیوس؛ −۳۴۱ درجه فارنهایت) ضدفرومغناطیس است (حالت متوسط) و در نهایت در دمای بالاتر از ۱۶۰ کلوین (−۱۱۳ درجه سلسیوس؛ −۱۷۲ درجه فارنهایت) پارامغناطیس میشود (زمینهها و عوامل مغناطیسی خارجی میتوانند آن را مغناطیسی کنند).[20]
در محیط
آثار کالیفرنیوم را میتوان در نزدیکی تأسیساتی یافت که از این عنصر در کاوش مواد معدنی و در معالجه پزشکی استفاده میکنند.[21] این عنصر در آب قابل حل نیست، اما به خوبی به خاک معمولی میچسبد؛ و غلظت آن در خاک میتواند ۵۰۰ برابر بیشتر از آب اطراف ذرات خاک باشد.[22]
نتیجه آزمایش هسته ای جوی قبل از سال ۱۹۸۰ مقدار کمی کالیفرنیوم به محیط زیست وارد کرد.[22] ایزوتوپهای کالیفرنیوم با تعداد جرم ۲۴۹، ۲۵۲، ۲۵۳ و ۲۵۴ در گرد و غبار رادیواکتیو جمع شده از هوا پس از انفجار هسته ای مشاهده شدهاست.[23] کالیفرنیوم از آنجا که در مقادیر زیادی تولید نشدهاست، یک رادیونوکلئید عمده در وزارت انرژی ایالات متحده نیست.[22]
زمانی تصور میشد کالیفرنیوم در ابرنواخترها تولید میشود، زیرا پوسیدگی آنها با نیمه عمر ۶۰ روزه 254Cf مطابقت دارد.[24] با این حال، مطالعات بعدی نتوانستند طیفهای کالیفرنیوم را نشان دهند،[25] و اکنون تصور میشود که منحنیهای سبک ابرنواختر از فروپاشی نیکل -۵۶ پیروی کنند.[26]
عناصر ترانس اورانیک از آمریسیم به فرمیوم، از جمله کالیفرنیوم، بهطور طبیعی در رآکتور شکافت هسته ای طبیعی در Oklo رخ دادهاند، اما دیگر چنین نمیکنند.[27]
کاربردها
فعالیتهای هستهای
یادداشت
- The Earth formed 4.5 billion years ago, and the extent of natural neutron emission within it that could produce californium from more stable elements is extremely limited.
منابع
- CRC 2006, p. 1.14.
- CRC 2006, p. 4.56.
- Joseph Jacob Katz; Glenn Theodore Seaborg; Lester R. Morss (1986). The Chemistry of the actinide elements. Chapman and Hall. p. 1038. ISBN 9780412273704. Retrieved 11 July 2011.
- Greenwood & Earnshaw 1997, p. 1265.
- Kovács, Attila; Dau, Phuong D.; Marçalo, Joaquim; Gibson, John K. (2018). "Pentavalent Curium, Berkelium, and Californium in Nitrate Complexes: Extending Actinide Chemistry and Oxidation States". Inorg. Chem. American Chemical Society. 57 (15): 9453–9467. doi:10.1021/acs.inorgchem.8b01450. PMID 30040397.
- Emsley 1998, p. 50.
- CRC 2006, p. 10.204.
- CRC 1991, p. 254.
- CRC 2006, p. 11.196.
- NNDC contributors (2008). Sonzogni, Alejandro A. (Database Manager), ed. "Chart of Nuclides". National Nuclear Data Center, Brookhaven National Laboratory. Retrieved 1 March 2010.
- Cunningham 1968, p. ۱۰۳.
- Street, K. , Jr.; Thompson, S. G.; Seaborg, Glenn T. (1950). "Chemical Properties of Californium" (PDF). Journal of the American Chemical Society. 72 (10): 4832. doi:10.1021/ja01166a528. hdl:2027/mdp.39015086449173.
- Glenn Theodore Seaborg (1990). Journal of Glenn T. Seaborg, 1946-1958: January 1, 1950-December 31, 1950. Lawrence Berkeley Laboratory, University of California. p. 80.
- Cunningham 1968, p. 103.
- Thompson, S. G.; Street, Jr., K.; A., Ghiorso; Seaborg, Glenn T. (1950). "Element 98". Physical Review. 78 (3): 298. Bibcode:1950PhRv...78..298T. doi:10.1103/PhysRev.78.298.2.
- Seaborg 1996, p. ۸۲.
- Jakubke 1994, p. ۱۶۶.
- Haire 2006, pp. ۱۵۲۲–۱۵۲۳.
- Haire 2006, p. ۱۵۲۶.
- Haire 2006, p. ۱۵۲۵.
- Emsley 2001, p. ۹۰.
- ANL contributors (August 2005). "Human Health Fact Sheet: Californium" (PDF). Argonne National Laboratory. Archived from the original (PDF) on 2011-07-21.
- Fields, P. R.; Studier, M.; Diamond, H.; Mech, J.; Inghram, M.; Pyle, G.; Stevens, C.; Fried, S.; et al. (1956). "Transplutonium Elements in Thermonuclear Test Debris". Physical Review. 102 (1): 180–182. Bibcode:1956PhRv..102..180F. doi:10.1103/PhysRev.102.180.
- Baade, W.; Burbidge, G. R.; Hoyle, F.; Burbidge, E. M.; Christy, R. F.; Fowler, W. A. (August 1956). "Supernovae and Californium 254" (PDF). Publications of the Astronomical Society of the Pacific. 68 (403): 296–300. Bibcode:1956PASP...68..296B. doi:10.1086/126941. Retrieved 26 September 2012.
- Conway, J. G.; Hulet, E.K.; Morrow, R.J. (1 February 1962). "Emission Spectrum of Californium". Journal of the Optical Society of America. 52 (2): 222. doi:10.1364/josa.52.000222. OSTI 4806792. PMID 13881026.
- Ruiz-Lapuente1996, p. ۲۷۴.
- Emsley, John (2011). Nature's Building Blocks: An A-Z Guide to the Elements (New ed.). New York, NY: Oxford University Press. ISBN 978-0-19-960563-7.
پیوند به بیرون
- کالیفرنیا در جدول دوره ای فیلمها (دانشگاه ناتینگهام)
- NuclearWeaponArchive.org - کالیفرنیا
- بانک اطلاعات مواد خطرناک - کالیفرنیا ، رادیواکتیو
| در ویکیانبار پروندههایی دربارهٔ کالیفرنیوم موجود است. |
