تریفلونوماید
تریفلونوماید (انگلیسی: Teriflunomide) متابولیت لفلونوماید است.[1] این دارو فاز سوم کارآزمایی بالینیِ TEMSO را برای درمان اماس در ژوئیه ۲۰۱۰ میلادی[2] پشت سر گذاشت و نتایج دوسالهٔ بهدستآمده، مثبت بودند.[3] با اینحال در کارآزمایی بالینیِ TENERE که مقایسهٔ شانهبهشانهٔ تریفلونوماید با اینترفرون بتا-۱ای بود، ثابت گردید که گرچه قطعِ دائمی درمان با تریفلونوماید کمتر رخ میدهد، اما میزان عود بیماری با آن شایعتر از درمان با اینترفرون بتا-۱ای است.[4]
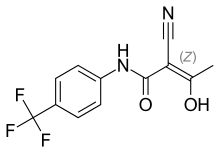 | |
|---|---|
 | |
| سامانهشناسی نام (آیوپاک) | |
| (2Z)-2-cyano-3-hydroxy-N-[4-(trifluoromethyl)phenyl]but-2-enamide | |
| دادههای بالینی | |
| نام تجاری | Aubagio |
| Licence data | EMA:Link, US FDA:link |
| رده بارداری | X(US) |
| تجویز | خوراکی (قرص) |
| دادههای فارماکوکینتیکی | |
| پیوند پروتئینی | بیش از ۹۹٫۳٪ |
| نیمهعمر | ۲ هفته |
| دفع | صفراوی/مدفوع، کلیوی |
| شناسه | |
| شماره سیایاس | 163451-81-8 |
| کد ATC | L04AA31 |
| پابکم | CID 54684141 |
| IUPHAR ligand | ۶۸۴۴ |
| کماسپایدر | 16737143 |
| UNII | 1C058IKG3B |
| KEGG | D10172 |
| ChEBI | CHEBI:۶۸۵۴۰ |
| ChEMBL | CHEMBL973 |
| مترادفها | A77 1726 |
| دادههای شیمی | |
| فرمول | C12H9F3N2O۲ |
| وزن مولکولی | 270.207 g/mol |
| SMILES | eMolecules & PubChem |
| |
| | |
این دارو در ۱۳ سپتامبر ۲۰۱۲ میلادی توسط سازمان غذا و داروی ایالات متحدهٔ آمریکا[5] و در ۲۶ اوت ۲۰۱۳ توسط اتحادیه اروپا تأیید شد.[6]
مکانیسم عمل
تریفلونوماید یک داروی ایمونوتراپی است که از ساخت پیریمیدین جدید را از طریق مهار آنزیم دیهیدرواوروتات دهیدروژناز، جلوگیری میکند. معلوم نیست که این موضوع، دلیلِ اثرات ضد اماس آن باشد.[7]
تریفلونوماید به سرعت جلوی تقسیم سلولی، از جملهلنفوسیتهای تی فعالشده را میگیرد که بروز بیماری اماس نقش مهمی دارند. خطر بروز عفونت با تریفلونوماید در مقایسه با داروهای شبه شیمیدرمانی کمتر است، چرا که اثرات محدودی بر روی دستگاه ایمنی بدن دارد.[8]
ثابت شده که تریفلونوماید NF-κB را مهار میکند. این دارو همچنین آنزیمهای تیروزین کیناز را نیز مهار میکند، اما این کار را در دوزهای زیاد انجام میدهد که کاربرد بالینی ندارند.[9]
منابع
- Magne D, Mézin F, Palmer G, Guerne PA (November 2006). "The active metabolite of leflunomide, A77 1726, increases proliferation of human synovial fibroblasts in presence of IL-1beta and TNF-alpha". Inflammation Research. 55 (11): 469–75. doi:10.1007/s00011-006-5196-x. PMID 17122964.
- ClinicalTrials.gov Phase III Study of Teriflunomide in Reducing the Frequency of Relapses and Accumulation of Disability in Patients With Multiple Sclerosis (TEMSO)
- "Sanofi-Aventis' Teriflunomide Comes Up Trumps in Two-Year Phase III MS Trial". 15 Oct 2010.
- Gever J (June 4, 2012). "Teriflunomide Modest Help but Safe for MS". medpage. Joint meeting of the Consortium of Multiple Sclerosis Centers and the Americas Committee for Treatment and Research in Multiple Sclerosis. Retrieved June 4, 2012.
- "FDA approves new multiple sclerosis treatment Aubagio" (Press release). US FDA. Retrieved 2012-09-14.
- EU authorisation details, EMA, retrieved 2014-04-29
- Spreitzer H (March 13, 2006). "Neue Wirkstoffe - Teriflunomid". Österreichische Apothekerzeitung (به German) (6/2006).
- Vollmer T (May 28, 2009). "MS Therapies in the Pipeline: Teriflunomide". EMS News (May 28, 2009).
- Breedveld FC, Dayer JM (November 2000). "Leflunomide: mode of action in the treatment of rheumatoid arthritis". Annals of the Rheumatic Diseases. 59 (11): 841–9. doi:10.1136/ard.59.11.841. PMC 1753034. PMID 11053058.
- مشارکتکنندگان ویکیپدیا. «Teriflunomide». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۱۸ اوت ۲۰۱۹.