خوردگی
خوردگی (به انگلیسی: Corrosion) یک فرایند طبیعی است که فلزات خالص شده را به اشکال پایدارتر شیمیایی مانند اکسید، هیدروکسید یا سولفید تبدیل میکند.[1] خوردگی بهطور کلی به صورت از بین رفتن مواد به علت واکنش با محیط تعریف میشود.
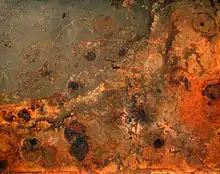
پدیده خوردگی طبق تعریف، واکنش شیمیایی یا الکتروشیمیایی بین یک ماده، معمولاً یک فلز، و محیط اطراف آن میباشد که به تغییر خواص ماده منجر خواهد شد. پدیده خوردگی در تمامی دستههای اصلی مواد، شامل فلزات، سرامیکها، پلیمرها و کامپوزیتها اتفاق میافتد، اما وقوع آن در فلزات آنقدر شایع و فراگیر بوده و اثرات مخربی به جای میگذارد که هرگاه صحبت از خوردگی به میان میآید، ناخودآگاه خوردگی یک فلز به ذهن متبادر میشود.
خوردگی معمولاً فرایندی زیانآور است، لیکن گاهی اوقات مفید واقع میشود. بهطور مثال آلودگی محیط به محصولات خوردگی و آسیب دیدن عملکرد یک سیستم از جنبههای زیانآور خوردگی و تولید انرژی الکتریکی در یک باتری و حفاظت کاتدی سازههای مختلف از فواید آن هستند، اما تأثیرات مخرب و هزینههای به بار آمده بواسطه این فرایند به مراتب بیشتر است.
تاریخچه
یکی از کهنترین آثار خوردگی مربوط به دیوار آهنی قفقاز است که به فرمان کورش هخامنشی ساخته شد و بدستور وی روی آن را با مس پوشش دادند. آغاز پژوهش به گونه امروزی در انگلستان پس از غرق شدن کشتی جنگی HMS Alarm در سال ۱۷۶۱ میلادی بود. پس از آن ورقههای مسی به بدنه کشتیها وصل میشد اما پس از چندی دیده شد که این ورقهها در جاهایی که میخهای فولادی آنها را نگه داشته بود، خورده شدهاند (خوردگی گالوانیک).
این دانش روزبه روز گستردهتر شد و امروزه شاخه مهمی در مهندسی و علوم پایه میباشد.
جایگاه آکادمیک
هر چند دانش مهندسی خوردگی در برخی از دانشگاههای دنیا از زیر شاخههای علم و مهندسی شیمی بوده و ارتباط تنگاتنگی نیز با آن دارد، در کشور ما سیاستگذاری در وزارت علوم، تحقیقات و فناوری بگونهای بودهاست که مهندسی خوردگی، از زیرشاخههای مهندسی مواد قرار داده شدهاست.
علم و مهندسی مواد که به شناخت ویژگیهای فیزیکی و مکانیکی مواد مختلف، روشهای ساخت آنها، روشهای استحصال فلزات و مواد نوین میپردازد، به لحاظ ساختار آکادمیک در کشور ما در مقطع کارشناسی دارای سه زیر شاخه مهندسی متالورژی صنعتی، مهندسی متالورژی استخراجی و مهندسی سرامیک است.
در مقطع کارشناسی ارشد، مهندسی مواد به زیرشاخههای انتخاب مواد مهندسی، شکلدهی فلزات، خوردگی، استخراج فلزات، سرامیک، بیومواد، ریختهگری و جوشکاری طبقهبندی شدهاست. با این توضیح مشخص است که برای تحصیل در رشته مهندسی خوردگی لازم است تا از مقطع کارشناسی در رشته مهندسی مواد آغاز کرد.
دانش خوردگی مواد، به ویژه فلزات همه صنایع را تحت تأثیر خود قرار داده و مهندسین این رشته همواره در تلاش هستند تا روشهای موجود برای مقابله با اثرات زیانبار این پدیده را بهبود بخشیده یا روشهای نوینی برای این کار بیابند. از آنجا که گستره نفوذ خوردگی در صنایع بسیار وسیع است، بنظر میرسد آشنایی با اصول و مبانی فرایند خوردگی و همچنین روشهای عمومی برای کنترل این پدیده برای همه مهندسین ضروری است.
انواع خوردگی و مکانیسم پدید آمدن آنها

خوردگی یکنواخت
در این نوع خوردگی واکنشهای شیمیایی بهطور یکنواخت در سطح فلزات با جابجایی پیوسته آند و کاتد ایجاد شده که علت آن پلاریزاسیون میباشد. بهطور مثال اغلب خوردگیهای فولاد از این نوع میباشد. اهمیت و قدرت این نوع خوردگی از دیگر انواع خوردگیها کمتر است.
خوردگی گالوانیکی
هر گاه دو فلز غیر هم جنس در یک الکترولیت تشکیل یک پیل خوردگی دهند، خوردگی گالوانیکی حاصل میشود. علت ایجاد این نوع خوردگی در بین فلزات را میتوان به اختلاف پتانسیل الکتروشیمیایی آنها نسبت داد. پتانسیل دو فلز در الکترولیتهای مختلف نسبت به یکدیگر متفاوت است. سرعت خوردگی به نسبت سطح کاتد/آند بستگی داشته و هر چه سطح کاتد بزرگتر از آند باشد، سرعت خوردگی و از بین رفتن آند بیشتر است. مثال پوشش دادن فولاد با لایهای از قلع یک نمونه از این خوردگی میباشد. اگر خراش یا شکافی در سطح خارجی قطعهٔ فولادی قلع اندود شده ایجاد شود، بهطوریکه فولاد به هوای محیط ارتباط پیدا کند، خوردگی در فولاد به وجود آمده و قلع سالم باقی میماند. اما درصورت عدم حضور اکسیژن هوا، قلع نسبت به فولاد آند را تشکیل میدهد و در این حالت قلع مادهٔ پوششی مناسبی برای فلزات از جمله ظروف غذایی و آشامیدنی فولادی (استیل) خواهد بود. پس در نتیجه اکسیژن عامل مهمی در در خوردگی گالوانیکی دارد.
خوردگی حفره ای

خوردگی حفرهای نوعی خوردگی موضعی است که به دنبال آن حفرههایی در سطح فلز ظاهر شده و با ادامه فعل انفعال خوردگی حفره عمیقتر شده و باعث سوراخ شدن لولهها میگردد. این نوع خوردگی برای سازههای مهندسی بسیار مخرب است. ناخالصیهای غیر فلزی، ناهمگنیهای ساختاری و شیمیایی در سطح فلز نقاط متداول مناسبی برای آغاز این نوع خوردگی و شروع ایجاد حفره است.
خوردگی شکافی (Crevice corrosion)
خوردگی شکافی، نوعی از خوردگی الکتروشیمیایی موضعی است که در شکافها و در زیر سطوح فلزی پوشش داده شده (به عنوان لایهٔ محافظتکننده)، در جایی که محلولهای راکد وجود دارد، اتفاق میافتد. این نوع خوردگی در بسیاری از سیستمهای آلیاژی مانند فولاد زنگ نزن و آلیاژهای تیتانیم، آلومینیم رخ میدهد. مکانیزم خوردگی شکافی تا حدود زیادی مشابه با مکانیزم خوردگی حفرهای است. این نوع خوردگی بیشتر میتواند در زیر واشرها، میخ پرچها، پینها، دریچهٔ شیرها محل تکیه گاهها و یاتاقانها و زیر رسوبات متخلخل و دیگر موقعیتهای مشابه به وجود آید.
خوردگی بین دانهای (Intergranular corrosion)

این نوع خوردگی که در مرز دانهها اتفاق میافتد از انواع خوردگی موضعی میباشد. طی فرایند انجام، مرز دانهها آخرین نقاطی هستند که منجمد میشوند، لذا غلظت عناصر آلیاژی و ناخالصی در مرز دانه فلزات بیشتر است. اختلاف غلظت آلیاژی بین سطح و مرز دانهها باعث اختلاف انرژی و در نتیجه تمایل به خورده شدن سطح و مرز دانهها میشوند و در نهایت مرز دانهها آند و سطح دانهها کاتد میشود. برای مثال آلیاژهای آلومینیم با استحکام بسیار بالا و تعدادی از آلیاژهای مس که شامل فازهای رسوبی در مرز دانهها برای افزایش استحکام است میتوانند تحت شرایط معینی برای خوردگی بین دانهای مستعد باشند.
خوردگی تنشی (Stress corrosion)
خوردگی تنشی نتیجه تأثیر همزمان تنشهای مکانیکی محیط خورندهٔ مناسب بر روی فلز است. این تنشهای مکانیکی میتواند ناشی از تنشهای خارجی یا داخلی (پسماند) باشد. تنش پسماند در حد بالا میتواند از تنشهای حرارتی در نتیجه سرد کردن غیر یکنواخت (سریع)، طراحی مکانیکی ضعیف برای تنشها، تبدیل فاز هنگام عملیات حرارتی، تغییر شکل سرد و جوشکاری باشد.
مکانیزم تخریب در خوردگی تنشی
مکانیزم تخریب در خوردگی تنشی ا آنجایی که سیستمهای بسیار مختلفی از آلیاژها و محیطهای خورنده وجود دارد بسیار پیچیدهاست. در موارد بسیاری تخریب از یک حفره یا ناپیوستگی دیگر موجود بر روی سطح فلز شروع و گسترش مییابد. در جدول زیر تعدادی از محیطهایی که میتواند موجب خوردگی تنشی فلزات و آلیاژها شوند آمدهاست.
خوردگی توأم با خستگی
خوردگی توأم با خستگی نوع دیگری از خوردگی است که در آن نقطه فلزی تحت تأثیر همزمان واکنش شیمیایی و بار دینامیکی (متناوب) قرار میگیرد. در نتیجهٔ این فعل و انفعال ترکهای درون دانهای ظاهر میشود، که شبیه به ساختار میکروسکوپی ترکها در شکست دائم خواهد بود.
خوردگی فرسایشی (Erosion corrosion)
فعل و انفعالاتی که به جدا شدن قسمتی از سطح فلز شده و در نتیجه شتابی در سرعت تهاجم خوردگی فلز که در ارتباط با حرکت نسبی مایع و یاز گاز خورنده در سطح تماس فلز میانجامد به عنوان خوردگی فرسایشی تعریف میشود.
خوردگی سایشی (Fretting corrosion)
خوردگی در اثر سایش ناشی از حرکت سیال تشدید میشود. با افزایش مواد جامد در سیال این نوع خوردگی تشدید میشود. سایش باعث از بین رفتن محصولات خوردگی ایجاد شده در سطح فلز میشود و به الکترولیت اجازه تماس با سطح فلز جهت ادامه خوردگی را میدهد. بهطور مثال سرعت گردش سیال حفاری، میزان مواد جامد گِل و جریان آشفته سیال حفاری از عواملی هستند که نسبت مستقیم با این نوع خوردگی دارند.
خوردگی غلظتی (Concentration corrosion)
خوردگی زیر رسوبات نام دیگر این نوع خوردگی میباشد. خوردگی اکسیژنی نیز از انواع خوردگی غلظتی است. بهطور مثال پوشیده شدن قسمتی از سطح لولههای حفاری توسط گِل، محصولات خوردگی و لاستیک حلقوی محافظ لولهها باعث ایجاد این نوع خوردگی میشود، اختلاف غلظت اکسیژنی ناحیه پوشیده شده توسط رسوبات و ناحیه آزاد باعث شده که سطح زیر این رسوبات آند و بقیه لوله کاتد شود.
خوردگی روی زدایی (Dezincification corrosion)
یکی از انواع خوردگی است که در آلیاژهای مس – روی اتفاق میافتد. در آلیاژهای (برنز و برنج) هر دو فلز مس و روی وارد الکترولیت شده سپس مس مجدداً سطح نمونه را پوشانده و روی در محلول باقی میماند، به این علت در صورتیکه این آلیاژها مدتی در محیط خورنده قرار گیرند سطح فلز قرمز و متخلخل میشود. به این فرایند روی زدایی گویند.
خوردگی در اثر فلزات مذاب
این نوع خوردگی بیشتر در بعضی از راکتورهای اتمی دیده میشود. در بعضی از رآکتورها از فلزات مذاب مانند سدیم به عنوان وسیلهٔ خنککننده استفاده میشود، زیرا که سدیم قابلیت هدایت حرارتی خوبی دارد. در اینجا واکنش خوردگی عمدتاً مسئله انتقال جرم است و به خوردگی موضعی مربوط نمیشود. علت پدیدار شدن این نوع خوردگی تمایلی است که ذرات جسم برای حل شدن در فلز مذاب دارند. این تمایل تا موقعی که در درجه حرارت معین به حد حلالیت و در نتیجه حالت تعادل برسد برقرار است. تأثیر تهاجم خوردگی در نتیجه فلزات مذاب میتواند به صورتهای مختلف مانند حل شدن ساده فلزات، تشکیل ترکیب شیمیایی، متلاشی شدن موضعی اجزایی از فلز باشند.[2]
عوامل مؤثر بر خوردگی
درجه حرارت
حرارت محیط یکی از عواملی است که بر میزان و شدت خوردگی فلزات تأثیرگذار میباشد. افزایش درجه حرارت محیط باعث افزایش سرعت خوردگی میشود. به صورت تجربی مشاهده شدهاست که با افزایش هر ۱۰ درجه حرارت محیط سرعت خوردگی فلز ۲ برابر میشود.
اختلاف پتانسیل
در یک محیط الکترولیتی مشترک اگر دو فلز از جنسهای متفاوتی وجود داشته باشد از آنجا که به صورت الکترود در می ایند، اختلاف پتانسل بین آنها شکل میگیرد که باعث میشود بسته به جنس فلز یکی تبدیل بهاند و دیگری تبدیل به کاتد گردد. در این حالت فلز اندی با سرعت بیشتری شروع به خورده شدن میکند.
خواص فلزی

ساختمان درونی فلزات از عوامل مهمی است که بر روی خوردگی فلزات و شدت ان تأثیر قابل توجهی دارد. ساختاربلوری فلز، نوع آلیاژ و ترکیب شمیایی ان، روشهای ریختهگری، خواص مکانیکی و مقاومتی فلزات و انواع مختلف الیاژها و عملیات حرارتی ازمواردی است که بر میزان خوردگی تأثیرگذار میباشد.
عوامل مکانیکی
یکی از موارد مؤثر بر خوردگی ساییدگی است. ساییدگی سطح فلز باعث میگردد لایههای اولیه خورده شده بر روی سطح فلز که مانع از خوردگی سطحهای پایینتر ان میگردد، از بین رفته و سطحهای پایینتر در معرض خوردگیهای بعدی قرار گیرد. مورد مؤثر دیگر برای قطعات فلزی است که تحت تأثیر تنشهای کششی هستند مخصوصاً زمانی که تنشها از قدرت ارتجاعی فلز بالاتر باشند. در این حالت آمادگی فلز برای خوردگی بسیار بالا میباشد. فطعات فلزی که تخت فشار میباشند نیز در معرض خوردگی بیشتر قرار دارند.
ناخالصیها و شرایط محیطی
رطوبت خود عامل مهمی در خوردگی فلزات است زیرا الکترولیتی را برای ایجاد محیط اندی و کاتدی فراهم میآورد. از طرف دیگر وجود نمکها و ناخالصیها سرعت خوردگی را افزایش میدهند زیرا ایجاد محلول الکترولیتی میکنند که تبادل الکترون بین مواد شرکتکننده در خوردگی راحتتر اتفاق میافتد. pH نیز برروند خوردگی تأثیرگذار است. محیط اسیدی الکترولیت قویتری ایجاد خواهد کرد و در نتیجه سرعت خوردگی افزایش پیدا خواهد کرد. از طرف دیگری ایجاد اختلاف مقداری pH در فسمتهای مختلف فلز باعث به وجود امدن محیطهای اندی و کاتدی می گردد که در روندخوردگی تأثیرگذار خواهند بود.[3]
هزینههای خوردگی

از آنجا که خوردگی پدیدهای تخریبی است، هزینههایی در پی دارد. این هزینهها در دو دسته مستقیم و غیر مستقم (پیامدهای مستقیم) هستند که دسته دوم بسیار بیشتر از نخستین است. در آمریکا در سال هزینه سالانه خوردگی چیزی پیرامون ۱/۳٪ تولید ناخالص داخلی (۲۷۷ میلیارد دلار در سال 1998])[4]
سرعت خوردگی
سرعت خوردگی (icorr)را با مقدار الکترون تولیدی بر یکای زمان (آمپر I) میتوان سنجید اما از آنجا که اثر سطح را باید در نظر داشت، بایستی عدد بدست آمده بر یکای سطح بخش گردد.
سرعت خوردگی بهطور معمول به صورت میل در سال (mpy) بیان میشود:
- که در آن W، کاهش وزن بر حسب میلیگرم، D چگالی نمونه بر یکای گرم بر سانتیمتر مکعب، A مساحت نمونه بر حسب اینچ مربع و T زمان خوردگی بر یکای ساعت است.[5]
| در ویکیانبار پروندههایی دربارهٔ خوردگی موجود است. |
خوردگی میکروبی (MIC)
عبارت microbiologically influenced corrosion(MIC) مربوط به نوعی از خوردگی یا تخریب ناشی شده یا گسترش یافته توسط فعالیتهای زندگی میکروبی است. MIC یک مکانیزم خوردگی جدید نیست اما شامل نقش میکروارگانیسمها در پروسه خوردگی است .MIC یک پروسه غیر زنده (abiotic) است تحت تأثیر فاکتورهای زنده بیولوژیکی (biotic).
تعریف دیگری از MIC بدین صورت است: اثر میکروارگانیسمها بر روی سینتیک پروسه خوردگی فلزات بواسطه چسبیدن آنها به فصل مشترک که معمولاً بیوفیلم خوانده میشوند. بعبارتی پیشنیاز MIC حضور و رشد میکروارگانیسم هاست.
پیشنیازهای خوردگی میکروبی
یک میکرو ارگانیسم برای آغاز متابولیسمش نیاز به انرژی و برای رشد نیاز به مواد مغذی مانند کربن، نیتروژن و فسفر دارد؛ بنابراین پیشنازهای MIC بدین صورت است:
- یک منبع انرژی
- یک منبع کربن
- یک دهنده الکترون
- یک پذیرنده الکترون
- آب
انرژی مورد نیاز ممکن است از نور خورشید و طی فرایند فتوسنتز گرفته شود یا از طریق واکنشهای شیمیایی اکسیداسیون و احیاء.
بسته به نوع تجهیزات منبع تأمین انرژی متفاوت خواهد بود برای تجهیزات قرار گرفته روی سطح زمین و نیز سیستمهای زیر آبی نور خورشید منبع تأمین انرژی است و برای تجهیزات بسته و زیر خاک انرژی مورد نیاز از واکنشهای شیمیایی تأمین میشود.
نور یک منبع مهمی از انرژی میباشد چرا که فرایند فتوسنتز را پیش میبرد (در فتوسنتز دیاکسید کربن و آب مصرف و اکسیژن و هیدراتهای کربن به وجود میآیند).
تحت شرایط هوازی احیاء اکسیژن به آب کاملکننده فرایند متابولیکی تبدیل مواد مغذی به دیاکسید کربن است و تحت شرایط بیهوازی پذیرندههای دیگری غیر از اکسیژن وارد واکنش میشوند.
لازم است ذکر شود که MICتنها زمانی میتواند اتفاق بیفتد که میکروارگانیسمها فعال و حاضر باشند. میکرو ارگانیسمها بیش از هر چیزی نیاز به آب دارند. اگر که اکتیویته آب کمتر از ۰٫۹باشد باکتریها نمیتوانند رشد کنند. تنها قارچ هامی توانند در آبی با اکتیویته ۰٫۷رشد کنند، اما آنها نقش مهمی در MICبازی نمیکنند.
بیوفیلم SRB و رفتار خوردگی آن
SRBیک ترم عمومی است شامل تمام تک سلولیهایی میشود که سولفات(SO4 2-) سولفید و تیوسولفات و همچنین گوگرد را برای بدست آوردن انرژی به H2S احیا میکنند. برای انواع باکتریهای متفاوت مناسبترین دما برای رشدSRB حدود۲۰–۳۰ است؛ ولی این باکتریها قادرند تا دمای ۵۰–۶۰˚Cنیز زنده بمانند .SRB به عنوان اصلیترین عامل MIC در آهن، مس و آلیاژهای آهنی شنا خته شدهاست. SRBدر شرایط بیهوازی خاک، آب دریا، فاضلاب، لولههای زیر زمینی و چاههای نفت با pHهای بین ۶–۹ وابسته است.
SRBهمه جا یافت میشوند، بی هوازیهای بسیار متفاوتی هستند (در ضمن بیماریزا نیستند). متداولترین آنها Desulfovibrioاست. یک میکرو ارگانیسم میتواند به راحتی به سطح بچسبد لایههایی را به نام بیو فیلم تشکیل دهد، بدین صورت که ابتدا بخشهای آلی روی سطح مواد میچسبند. میکروارگانیسمها خواص سطحی مواد بخصوص بار استاتیکی و قابلیت خیس شوندگی آن را تغییر میدهند. سپس باکتریها جذب سطح میشوند و رشد میکنند تا کلونیها را تولید کنند، بنابراین میکرو فیلمها رشد خواهند کرد. این لایهها میتوانند خیلی نازک باشند یا رشد کنند و به ضخامت سانتیمتر هم برسند. بیوفیلمها با یک ساختار غیر یکنواخت شناخته میشوند.
گرچه SRB بیهوازی هستند میتوانند در غلظتهای کمی از اکسیژن نیز رشد کنند. فعالیت SRBدر سیستمهای طبیعی و انسانی باعث ایجاد نگرانی در صنایع شدهاست. بخصوص در صنایع نفت و گاز و کشتیسازی که شدیداً به وسیلهٔ سولفید تولید شده توسط SRB تحت تأثیر قرار میگیرند.
راههای پیشگیری از خوردگی
روشهای جلوگیری از خوردگی یکنواخت
خوردگی یکنواخت را به سه طریق میتوان کنترل یا کم کرد که ممکن است یک نوع یا دو نوع را با همدیگر انجام داد.
- انتخاب مواد و پوشش صحیح
- به وسیله ممانعتکنندهها
- استفاده از حفاظت کاتدی
روش جلوگیری از خوردگی گالوانیکی
برای جلوگیری از این خوردگی روشهای مختلفی وجود دارد که گاهی یکی به تنهائی پاسخگو نمیباشد و باید دو یا سه نوع را با هم به کار برد.
- حتیالامکان سعی شود از دو فلز که در جدول سری الکتروشیمیائی فاصله کمتری نسبت به هم دارند استفاده شود.
- از نسبت سطحی نامطلوب، آند کوچک و کاتد بزرگ پرهیز شود. مخصوصاً در اتصالات
- از خاصیت عایقها دو فلز غیرهمجنس استفاده شود.
- استفاده از پوششها مخصوصاً روی آند
- استفاده از ممانعتکنندهها
- در مورد موادی که در جدول گالوانیکی دور از یکدیگر میباشند از اتصالات پیچ و مهره بپرهیزید. به دلیل کم شدن ضخامت مؤثر در مرحله پیچسازی سعی شود ازاتصال زرد جوش BRAZING استفاده شود.
- قسمتهای آندی را طوری طراحی کنید که به سهولت قابل تعویض باشند یا آنها را ضخیمتر انتخاب کنید تا عمر بیشتری داشته باشند.
- به اتصالهای گالوانیکی، فلز سومی که نسبت به دو فلز قبلی آند باشد متصل نمائید. (آند فداشونده)
روشهای جلوگیری از خوردگی شیاری
- شیارها را در محل روی هم قرار گرفتن دو فلز با جوشکاری مداوم، کالک کردن CAULKING یا لحیمکاری بپوشانید.
- از تهنشین شدن مواد و تجمع آنها در کف تانکها و مخازن جلوگیری شود.
- از ایجاد گوشههای تیز و نواحی مرده و ساکن در تجهیزات بپرهیزید.
- بازرسی و تمیز تمودن مرتب تجهیزات
- حذف جامدات معلق در فرایند کارخانهها
- در مرحله خوابیدن کارخانه، مواد جاذب رطوبت WET PACKING MATERIALS را حذف نمائید.
- در صورت امکان، محیط یکنواخت به وجود بیاورید مثلاً در پشت بند BACKFILL کردن یک خط لوله.
- هر جا که ممکن باشد از واشرهای جامد که جاذب رطوبت نیستند NONABSOKBENT مانند تفلون استفاده نمائید.
روشهای جلوگیری از خوردگی حفرهای
- کلیه روشهائی که برای مبارزه با خوردگی شیاری ذکر گردید در این نوع خوردگی نیز مؤثر میباشد.
- استفاده از آلیاژهائی که در برابر حفرهدار شدن بسیار مقاوم میباشند.
این نوع آلیاژها عبارتند از:
- فولاد زنگ نزن نوع ۳۰۴
- فولاد زنگ نزن نوع ۳۱۶
- هستولیF، نیونل یا دوریمت ۲۰
- هستولی C، یا کلریمت ۳
- تیتانیم
نکته: افزودن ممانعتکننده باید با دقت خاصی صورت گیرد به دلیل اینکه اگر خوردگی کاملاً متوقف نگردد، حفرهدار شدن تشدید میشود.
روشهای جلوگیری از خوردگی بیندانهای
به دلیل اینکه این خوردگی بیشتر در فولادهای زنگ نزن اتفاق میافتد سه روش جلوگیری آن را در این مورد ذکر میکنیم:
- در درجه حرارت بالا فلز تحت عملیات حرارتی محلولی قرار داده شود و سپس در آب سریع سرد شود.
- اضافه کردن عناصری که تمایل شدیدی به واکنش و یکنواخت کردن آلیاژ دارند این عناصر را پایدارکنندهها مینامند.
- تقلیل کربن فولاد به کمتر از ۰۳/۰ درصد تا کاربید کافی برای به وجود آمدن خوردگی بین دانهای به وجود نیاید. عملیات حرارتی محلولی در صنعت، مشتمل بر حرارت دادن در ۱۰?۰ درجه سانتگراد تا ۱۱?۰ و سپس سرد کردن سریع در آب میباشد. در این درجه حرارتها کاربید کرم حل میشود و در نتیجه آلیاژ همگنتر و یکنواختتر به دست میآید.
روشهای جلوگیری از جدایش انتخابی
- کم کردن خوردگی محیط مثلاً حذف اکسیژن
- حفاظت کاتدی
- اضافه کردن فلزی دیگر به آلیاژ. مثلاً اضافه کردن ۱٪ درصد قلع به برنج ۳۰–۷۰
- استفاده از ممانعتکننده مانند افزودن مقادیر کمی آرسنیک و آنتیموان یا فسفر به آلیاژ برنج
- برای محیطهائی بسیار خورنده که زدایش روی در آنها اتفاق میافتد یا برای قطعاتی که از اهمیت بالائی برخوردارند و نباید به هیچ وجه خورده شوند از کوپرونیکلها استفاده میکنند.
روشهای جلوگیری از خوردگی سایشی
پوششهای سخت یا زرهها یا روکشهای قابل تعویض، مشروط به اینکه از جنس مقاومی از نظر خوردگی ساخته شده باشند کاربرد مفیدی در خوردگی سایشی دارد.
روشهای جلوگیری از خوردگی همراه با تنش
- کم کردن تنش تا زیر حد مجاز مثلاً با کم کردن باروی فلز یا ضخیمتر کردن قطعه
- حذف اجزا و ناخالصیهای مضر محیط مانند دگازه کردن، دهینداله کردن یا تقطیر نمودن.
- استفاده از آلیاژ مناسب مثلاً استفاده از اینکونل که دارای مقدار نیکل بیشتر میباشد به جای فولاد زنگ نزن
کاربرد حفاظت کاتدی
این مورد باید مواقعی به کار برده شود که مطمئن باشیم خوردگی در اثر SCC بودهاست نه در اثر تردی هیدروژنی، زیرا در غیر این صورت حالت عکس دارد.
- اضافه کردن ممانعتکنندهها به سیستم در صورت امکان
- در محیطهای خورنده متوسط، فسفاتها و ممانعتکنندههای آلی و معدنی دیگر بهطور موفقیتآمیزی SCC را کاهش میدهند.
- ساچمهزنی (شات بلاست کردن) مثلاً فولاد زنگ نزن؟ ۱۰ در معرض محلول ۳٪ نمک طعام در دمای محیط با نوع ۳۰? در معرض محلول؟ ۲٪ کلرور منیزیم در ۱?۰ و آلیاژ آلومینیوم 7075-T6 در محلول در دمای محیط
- ساچمهزنی یا شات بلاست کردن عبارت است از ایجاد یک لایه پوسته مناسب در شرایط خاص بر روی فلزات و آلیاژهاو اینکونل (یکی از آلیاژهای نیکل) INCONEL است.
منابع
Hamidreza Mansouri, Seyed Abolhasan Alavi, Meysam Fotovat, "Microbial Influenced Corrosion of Corten Steel Compared to Carbon Steel and Stainless Steel in Oily Waste Water by Pseudomonas Aeruginosa"; JOM
- "Corrosion". Wikipedia. 2019-12-05.
- http://www.jgt-ndt.com
- http://www.jgt-ndt.com/عوامل-موثر-در-خوردگی/
- انجمن بینالمللی مهندسان خوردگی
- حسین قلی زادگان. «اصول خوردگی». دریا تامین. بایگانیشده از اصلی در ۱ نوامبر ۲۰۱۶. دریافتشده در ۱۱ آبان ۱۳۹۵.
Mars G. Fontana, Corrosion Engineering, McGraw-Hill,.

