زیرکونیوم کاربید
زیرکونیوم کاربید (به انگلیسی: Zirconium carbide) با فرمول شیمیایی ZrC یکی از مهمترین سرامیکهای دارای خصوصیات برتر از جمله نقطه ذوب بالا در مقایسه با زیرکونیوم نیترید، سختی بالا، پایداری مکانیکی جالب، تابع کار پایین و رفتار فلز گونه در خصوصیات الکتریکی و اپتیکی میباشد.[3]
Zirconium carbide
 | |
|---|---|
 | |
دیگر نامها zirconium(IV) carbide | |
| شناساگرها | |
| شماره ثبت سیایاس | ۱۲۰۷۰-۱۴-۳ |
| خصوصیات | |
| فرمول مولکولی | ZrC |
| جرم مولی | 103.235 g/mol |
| شکل ظاهری | gray refractory solid |
| چگالی | 6.73 g/cm3 |
| دمای ذوب | ۳۵۳۲ °C |
| دمای جوش | ۵۱۰۰ °C |
| انحلالپذیری در آب | insoluble |
| انحلالپذیری | soluble in concentrated سولفوریک اسید، هیدروفلوئوریک اسید، نیتریک اسید |
| ساختار | |
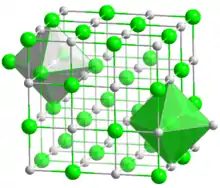
| ساختار بلوری | سدیم کلرید، cF8 |
| گروه فضایی | Fm3m No. 225 |
| Octahedral | |
| ترموشیمی | |
آنتالپی استاندارد تشکیل ΔfH |
-207 kJ/mol (extrapolated to stoichiometric composition)[2] |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
خواص
شکل ظاهری آن یک پودر فلزی خاکستری با ساختار بلور مکعبی و جرم مولی 103.235 g/mol میباشد. زیرکونیوم کاربید بسیار مقاوم در برابر خوردگی است. این کاربید فلزی بینابینی گروه IV همچنین عضوی از سرامیکهای با درجه حرارت فوقالعاده بالا یا (UHTC) است. به دلیل وجود پیوند فلزی ZrC دارای هدایت حرارتی w/m.k 5/20 و هدایت الکتریکی (مقاومت ~ μΩ.cm 43) است که هر دو مشابه فلز زیرکونیوم هستند. پیوند کووالانسی قوی Zr-C به این ماده یک نقطه ذوب بسیار بالا (۳۵۳۰ درجه سانتیگراد)، مدول بالا (GPa 440) و سختی (GPa 25) میدهد. ZrC در مقایسه با سایر کاربیدها مانند WC (15.8 g / cm3)، TaC (14.5 g / cm3) و HfC (12.67 g / cm3) چگالی کمتری دارد (6.73 g / cm3). مانند بیشتر کاربیدهای فلزات نسوز، کاربید زیرکونیوم زیر استوکیومتری است، یعنی حاوی جای خالی کربن است. در محتوای کربن بالاتر از تقریباً ZrC0.98، ماده حاوی کربن آزاد است.[2] ZrC برای نسبت کربن به فلز از ۰٫۶۵ تا ۰٫۹۸ پایدار است.
کاربرد
استفاده از پوششهای فلزی، معدنی، آلی و کامپوزیتی در سطح فلز با هدف افزایش مقاومت خوردگی فلزات بسیار معمول است. در این میان، پوششهای کاربیدی به دلیل خصوصیات منحصر به فرد مانند سختی و نقطه ذوب بالا و پایداری شیمیایی مناسب مورد توجه زیادی قرار گرفته شدهاست. کاربید زیرکونیوم (ZrC) یکی از کاربیدهای فلزی است که که به دلیل نقطه ذوب بالا (۳۵۵۰ درجه سانتیگراد)، سختی بالا، مقاومت در برابر سایش، هدایت الکتریکی بالا، پایداری شیمیایی و مقاومت خوردگی مناسب، به عنوان یک گزینه مطرح برای ایجاد پوششهای مقاوم به خوردگی است.[4] از پوششهای ZrC تا حد زیادی به عنوان مواد نسوز، ابزار برش، بوته در صنایع مکانیکی و هسته ای و همچنین در دستگاههای الکترونیکی استفاده میشود.[5]
مقاومت ضعیف در برابر اکسیداسیون بیش از ۸۰۰ درجه سانتیگراد، کاربردهای ZrC را محدود میکند. یکی از راههای بهبود مقاومت در برابر اکسیداسیون ZrC ساخت کامپوزیت است. کامپوزیتهای مهم پیشنهادی کامپوزیت ZrC-ZrB2 و ZrC-ZrB2-SiC هستند. این کامپوزیتها میتوانند تا دمای ۱۸۰۰ درجه سانتیگراد کار کنند. کاربید زیرکونیوم بدون هافنیوم و کاربید نیوبیوم میتوانند به عنوان پوشش نسوز در راکتورهای هسته ای استفاده شوند. به دلیل سطح مقطع جذب نوترون کم و حساسیت ضعیف به آسیب تحت تابش، به عنوان پوشش دیاکسید اورانیوم و ذرات دیاکسید توریم سوخت هسته ای استفاده میشود. این پوشش معمولاً با رسوب بخار شیمیایی حرارتی در یک راکتور بستر سیال رسوب میکند. این ماده همچنین دارای انتشار و ظرفیت جریان بالا در دمای بالا است و آن را به عنوان ماده امیدوار کننده ای برای استفاده در رادیاتورهای حرارتی فتووالتائیک و نوارها و آرایههای ساطع کننده میدانی ارائه میدهد.
روش تولید
برای تهیه کاربید زیرکونیم از روشهای مختلف مانند رسوب بخار شیمیایی(CVD)، سل-ژل، روش غوطه وری در نمک مذاب، روش الکترولیز از نمک مذاب و سنتز حالت جامد استفاده میشود. در روش الکترولیز از نمک مذاب، با انتخاب یک الکترولیت مناسب متشکل از نمکهای مختلف در دمای بالا و اعمال چگالی جریان مشخص بر قطعه زیرکونیومی (به عنوان کاتد) پوشش کاربید زیرکونیوم در سطح قطعه ایجاد میشود. نمکهای بکار رفته حاوی نمک زیرکونیوم (تأمین کننده زیرکونیوم)، نمک کربنات (تأمین کننده کربن) و نمکهای تأمین کننده هدایت الکتریکی الکترولیت مذاب میباشند. چگالی جریان، زمان الکترولیز، حضور مواد افزودنی و ترکیب الکترولیت (نمک مذاب) از جمله عوامل مؤثر بر الکتروکریستالیزاسیون و در نتیجه کیفیت پوشش کاربیدی حاصل میباشند.[6] روش دیگر واکنش کربوترمال زیرکونیا توسط گرافیت است که منجر به ایجاد پودر میشود. سپس با زینتر پودر ZrC در دمای بالاتر از ۲۰۰۰ درجه سانتیگراد میتوان ZrC متراکم را ایجاد کرد. پرس گرم ZrC میتواند درجه حرارت زینتر را پایین آورده و در نتیجه به تولید ZrC کاملاً متراکم دانه ریز کمک میکند. از اسپارک پلاسما زینترینگ نیز برای تولید ZrC کاملاً متراکم استفاده میشود.[7] کاربید زیرکونیوم نیز میتواند با فرآوری مبتنی بر محلول ساخته شود.[8] که با واکنش اکسید فلز با استیل استون حاصل میشود.
عموماً از اختلاط پودری کربن (C) با فلز زیرکونیم (Zr)، هیبرید زیرکونیم (ZrH2) یا اکسید زیرکونیم (ZrO2) و واکنش احیای کربوترمال جهت استحصال پودر کاربید زیرکونیم استفاده میشود. به علت درشت دانه بودن و اختلاط مواد واکنش دهنده (مواد واکنش دهنده در مقیاس میکرون هستند)، دمای بسیار بالا جهت تشکیل کاربید مورد نظر در طول مدت احیای کربوترمال مورد نیاز میباشد. این شرایط باعث درشت دانه شدن کاربید حاصله نیز میشود؛ لذا معمولاً از پرس گرم برای تولید قطعات ZrC استفاده میکنند. اخیراً از روشهای نوینی جهت تولید کاربید زیرکونیم در دماهای پایینتر و با اندازه ذرات در مقیاس نانومتری مورد استفاده قرار گرفته که از این موارد میتوان به روشهای برپایه انحلال شیمیایی یا لایه نشانی به کمک پالس لیزر اشاره نمود. در روشهایی دیگر استفاده از واکنشهای درجا (in situ) یا استفاده از مواد اولیه ارزانتر مورد توجه قرار گرفتهاند. روشهای درجا معمولاً دارای فرآیندی ساده و قابل کنترل میباشند و همچنین استفاده از واکنش دهندههای ارزان قیمت و در دسترس از مزیتهای استفاده از چنین روشهایی میباشند. امکان طراحی شرایط برای این واکنشها جهت رسیدن به ذرات کاربیدی با اندازه ذرات در حد نانومتری از دیگر مزایای آن میباشد که بیش از پیش به بهبود خواص نانوپودر حاصله کمک میکند.
جستارهای وابسته
منابع
- Lide, David R. (1998), Handbook of Chemistry and Physics (87 ed.), Boca Raton, FL: CRC Press, pp. 4–96, ISBN 0-8493-0594-2
- Baker, Floyd B.; Storms, Edmund K.; Holley Jr., Charles E. (1969), "Enthalpy of formation of zirconium carbide", J. Chem. Eng. Data, 14: 244–246, doi:10.1021/je60041a034
- سیدی، هوشیار؛ مجتهدی زاده لاریجانی، مجید؛ برقعی، سید مجید؛ صادقی، مهدی (۱۳۹۱). «تهیه لایه نازک کاربید زیرکونیوم بر روی استییل 403 و مطالعه خواص نانو ساختاری و مکانیکی آن». نخستین کنفرانس سراسری فیزیک و کاربردهای آن.
- روحانی، رویا؛ عادل خانی، هادی؛ اسدی اسدآبادی، محسن؛ منجمی، مجید (۱۳۹۵). «مطالعه مقاومت خوردگی پوششهای نانو ساختار کاربید زیرکونیم». فصل نامه علمی پژوهشی علم و مهندسیی سرامیک.
- Liu، Chao؛ Liu، Bing؛ Shao، Youlin؛ Li، Ziqiang؛ Tang، Chunhe (۲۰۰۷). «Preparation and Characterization of Zirconium Carbide Coating on Coated Fuel Particles». The American Ceramic Society.
- روحانی، رویا؛ عادل خانی، هادی؛ اسدی اسدآبادی، محسن؛ منجمی، مجید (۱۳۹۵). «مطالعه مقاومت خوردگی پوششهای نانو ساختار کاربید زیرکونیم». فصل نامه علمی پژوهشی علم و مهندسی سرامیک.
- Wei، Xialu؛ Back، Christina؛ Izhvanov، Oleg؛ D. Haines، Christopher؛ A. Olevsky، Eugene (۲۰۱۶). «Zirconium Carbide Produced by Spark PlasmaSintering and Hot Pressing: Densification Kinetics,Grain Growth, and Thermal Properties». doi:10.3390/ma9070577.
- D. SACKS، MICHAEL؛ WANG، CHANG-AN؛ YANG، ZHAOHU؛ JAIN، ANUBHAV (۲۰۰۴). «Carbothermal reduction synthesisof nanocrystalline zirconium carbideand hafnium carbide powders usingsolution-derived precursors». MATERIALS SCIENCE.
- «IUPAC GOLD BOOK». دریافتشده در ۱۸ مارس ۲۰۱۲.
