داروپردازی
داروپردازی یا طراحی دارو (به انگلیسی: Drug design) فرایند طراحی یک دارو برمبنای یک هدف زیستیِ مشخص است. دارو معمولاً یک مولکول آلی است که کارکرد یک زیستمولکول را دستخوش تغییر میکند.
هدف دارو
هدف دارو زیستمولکولی است که در مسیرهای سوختوساز و پیامرسانی مختص به فرآیند یک بیماری خاص نقش دارد. زیستمولکولها با ارتباط با یکدیگر به واسطهی تعامل پروتئین-پروتئین و یا پروتئین-اسید نوکلئیک که به انتقال پیامها یا تغییرات متابولیکی منجر میشود، نقش مهمی در پیشرفت بیماری ایفا میکنند، بنابراین تنظیم عملکرد این زیستمولکولها میتواند برای جلوگیری از پیشرفت بیماری سودمند باشد.
برای تنظیم عملکرد زیستمولکولها سه راه وجود دارد: ۱. مهار عملکرد زیستمولکولها با استفاده از مولکولهای کوچک که با اتصال به آنها مانع از اتصال لیگاندها به آنها میشوند ۲. محدود کردن تعامل میان زیستمولکولها با استفاده از مولکولهای کوچک ۳. فعال کردن زیستمولکولهایی که عملکرد آنها در برخی بیماریها از قبیل سرطان مختل شده است. [1]
داروپردازی به کمک رایانه
کشف و توسعهی دارو نیازمند زمان و هزینهی زیادی است که میتوان آنها را به کمک رایانه به میزان چشمگیری کاهش داد. از داروپردازی به کمک رایانه میتوان در موارد زیر استفاده کرد: [2]
- پیشبینی و تخمین تمایل اتصال ترکیبات مختلف به هدف و امتیازدهی به ترکیبات مختلف بر اساس آن؛
- غربالگری مجازی در روشهای لیگاندبنیان و ساختاربنیان؛
- بهینهسازی میل به اتصال و انتخاب در ترکیبات پیشرو؛
- طراحی ترکیبات جدید از طریق اتصال قطعات ترکیبات مختلف و یا رشد یک مولکول اولیه؛
- ساخت مجموعه دادهها و کتابخانههایی با کیفیت بالا جهت استفاده در داروپردازی.
گونگان
طراحی دارو به دو صورت امکانپذیر است:
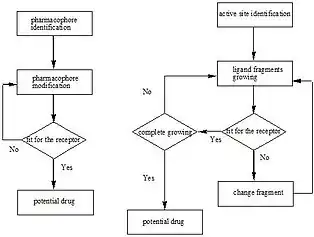
ساختاربنیان
روش ساختاربنیان یا داروپردازی مستقیم، روشی است که طی آن با درنظرگرفتن ساختار سهبعدی هدف زیستی، که معمولاً با کمک طیفبینی رزونانس مغناطیسی هستهای یا بلورشناسی پرتو ایکس تعیین میگردد، به طراحی دارو پرداخته میشود.
فرآیند داروپردازی ساختاربنیان شامل چندین چرخهی مکرر پیش از رسیدن به مرحلهی کارآزمایی بالینی است. اولین چرخه شامل شبیهسازی، خالصسازی و تعیین ساختار هدف زیستی به کمک بلورشناسی پرتو ایکس، طیفبینی رزونانس مغناطیسی هستهای و یا مدلسازی هومولوژی میباشد. اغلب پس از آن با استفاده از الگوریتمهای کامپیوتری، ترکیباتی از یک پایگاه داده در یک محیط شبیهسازی شده در یک ناحیهی مشخص از ساختار هدف قرار گرفته و بر اساس فعل و انفعالات الکترواستاتیک و موقعیت فضایی نسبت به هدف، امتیازدهی شده و بهترین آنها انتخاب میشوند. در چرخهی دوم موقعیتهایی از این ترکیبات که قابلیت بهینه شدن برای ارتقای توانایی دارو را دارند مشخص میشوند. درچرخههای بعدی فرآیند بهینهسازی ترکیبات و پیدا کردن هدفهای جدید به طور مکرر انجام میشود تا سرانجام ترکیبات بهینه و موثر روی هدف دارو پیدا شوند. [3] [4]
لیگاندبنیان
روش لیگاندبنیان یا داروپردازی غیرمستقیم، روشی است که طی آن با درنظرگرفتن مولکولهایی که تمایل به برقراری پیوند با هدف زیستی دارند، به طراحی دارو پرداخته میشود. با استفاده از این مولکولها یک مدل داروبر به دست میآید که حداقل ویژگیهای ساختاری را که یک مولکول برای اتصال به هدف نیاز دارد تعیین میکند. به عبارت دیگر با استفاده از دانش کسب شده در مورد مولکولهایی که به هدف اتصال پیدا میکنند، میتوان مدلی از هدف ارايه داد. از این مدل جدید میتوان برای طراحی عناصر مولکولی جدید که با هدف تعامل دارند استفاده نمود.
پانویس
- {Mandal, “Rational Drug Design”, European Journal of Pharmacology.
- {Tomar, “Small Molecule Drug Design”, Encyclopedia of Bioinformatics and Computational Biology.
- {Anderson, “The Process of Structure-Based Drug Design”, Chemistry and Biology.
- {Klebe, “Structure-based Drug Design”, Encyclopedic Reference of Genomics and Proteomics in Molecular Medicine.
منابع
- Mandal (۲۰۰۹). «Rational Drug Design». European Journal of Pharmacology. ۶۲۵: ۹۰–۱۰۰. doi:10.1016/j.ejphar.2009.06.065. PMID 19835861.
- Tomar (۲۰۱۹). «Small Molecule Drug Design». Encyclopedia of Bioinformatics and Computational Biology. ۳: ۹۷۴۱–۷۶۰. doi:10.1016/B978-0-12-809633-8.20157-X.
- Anderson (۲۰۰۳). «The Process of Structure-Based Drug Design». Chemistry and Biology. ۱۰: ۷۸۷–۷۹۷. doi:10.1016/j.chembiol.2003.09.002. PMID 14522049.
- Klebe (۲۰۰۶). «Structure-based Drug Design». Encyclopedic Reference of Genomics and Proteomics in Molecular Medicine. doi:10.1007/3-540-29623-9_0980.
