اولتراسوند سه بعدی
اولتراسوند سه بعدی یک روش تصویربرداری پزشکی است که معمولاً در تصویربرداری از جنین، قلب و کاربردهای ترانس رکتال و داخل عروقی استفاده میشود. سونوگرافی سه بعدی به صورت مشخص به نمایش حجمی از دادههای اولتراسوند (مافوق صوت) اشاره دارد. از سونوگرافی سه بعدی زمانی که در طی یک بازه زمانی یک سری تصویر گرفته شود به عنوان ۴ بعدی (سه بعد در فضا و یک بعد زمان) نیز یاد میشود.
هنگام تولید یک حجم سه بعدی، اطلاعات سونوگرافی سه بعدی را میتوان به ۴ روش معمول جمعآوری کرد:
با دست، که از طریق جهت دادن به پروب و دریافت یک سری تصویر اولتراسوند و ثبت جهت پروب برای هر برش انجام میشود.
مکانیکی، که جهت دهی به پروب خطی داخلی، از طریق یک موتور در درون پروب اصلی صورت میگیرد.
استفاده از یک اندوپروب (endoprobe)، که از طریق قرار دادن یک پروب و سپس برداشتن آن به صورت کنترل شده، حجم را ایجاد میکند.
مبدل به شکل آرایهٔ ماتریسی، که از جهت دادن موج به شکل هرم در جهت نقاط نمونه برداری استفاده میکند.[1]
خطرات
خطرات معمول در سونوگرافی معمولی نیز برای سونوگرافی سه بعدی برقرار است. اساساً سونوگرافی روشی ایمن در نظر گرفته میشود. در حالی که دیگر تکنیکهای تصویر برداری از مواد رادیواکتیو یا اشعههای یونیزهکننده استفاده میکنند، مبدلهای اولتراسوند، پالسهای صوتی با فرکانس بالا به بدن فرستاده و به بازگشت آن گوش میدهند.
بهطور خلاصه، ریسک اصلی در اولتراسوند به گرم شدن بافت یا حفره زایی برمی گردد. شیوهی اندازهگیری گرم شدن بافت و حفره زایی از طریق استانداردی به نام شاخص حرارتی [(thermal index(TI] و مکانیکی [(mechanical index(MI] انجام میگیرد. اگرچه FDA مقادیر بسیار ایمنی را برای حداکثر مقدار دو شاخص گفته شده مشخص کرده اما همچنان توصیه میشود از تصویربرداری سونوگرافی غیر ضروری خودداری شود.[2]
کاربردها
مامایی
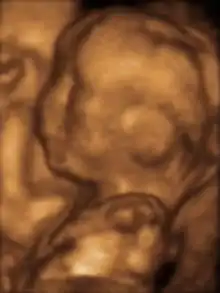
آزمایش مراحل رشد جنین در رحم به دلیل حرکت دائمی آن و تپش سریع قلب، کاریست سخت؛ بنابراین در هنگام تصویربرداری از رحم، نیاز است که شخص نفس خود را حبس کند تا تصویر واقعی را بتوان دریافت کرد. با سونوگرافی سه بعدی، پزشک میتواند حرکت جنین را در کسری از ثانیه تشخیص داده و اقدامهای لازم را به سرعت انجام دهد. علاوه بر تشخیص موقعیت جنین، مشکلات و رفتارهای غیرعادی در رحم مانند تجمع مایع یا هر انحنای ستون فقرات نیز قابل تشخیص است.[3] با سونوگرافی سه بعدی و پوشش سه بعدی، ضربان قلب جنین نیز قابل ردگیری بوده و پزشک را قادر به میکند روند رشد جنین را مشخص کند.[4]
قلب و عروق
کاربری سونوگرافی سه بعدی در درمانهای قلب پیشرفت قابل توجهی در تصویربرداری و درمان مشکلات قلبی کردهاست. زمانی که سونوگرافی سه بعدی برای نمایش وضعیت قلب استفاده شود، اکوکاردیوگرافی سه بعدی نامیده میشود.[5] با ترکیب تکنولوژیهای دیگر با اولتراسوند، اکنون اندازهگیریهای کمی مانند حجم محفظه قلب و همچنین اطلاعات مفید دیگری مانند رهگیری جریان خون یا سرعت انبساط و انقباض ممکن است.[6] با روش اکوکاردیوگرافی سه بعدی پزشکان اکنون میتوانند به راحتی بیماریهای شریانی را تشخیص داده و به دقت نواقص مختلف را بررسی کنند. کاربریهای پژواک (اکو) نیز به نمایش بیدرنگ ساختارهای قلب کمک میکند.[7]
هدایت در جراحی
در روشهای قدیمی اولتراسوند دوبعدی، محل دقیق بافتها و اعضا در جراحیها به خصوص در صفحه ای مورب قابل تشخیص نیست. با این حال، با پیدایش سونوگرافی سه بعدی و تکامل فضاهای قابل بررسی، جراح قادر به دریافت تصویر بیدرنگ از بافتها و اندامها بوده و میتواند اسکن کامل را بهتر تجسم کند.[8] علاوه بر این، سونوگرافی سه بعدی هدایت در جراحی را به شکل درمان پیوند و سرطان از طریق آشکارسازی چرخشی در زمان اسکن کردن ممکن میکند.[9] این تکنولوژی موجب تکامل روشهای متعددی مانند اسکن چرخشی، تصویر مقطعی، استفاده از مبدلهای آرایه ای مجتمع که به جراح برای کار با بیماران سرطانی سانحه دیده کمک میکند شدهاست.[10] به علاوه، پزشکان با سونوگرافی سه بعدی میتوانند انواع مختلفی از تومورها را به راحتی تشخیص و برای بررسی و مطالعهٔ معایب و دلایل از آن استفاده کنند.[11] بدین ترتیب میبینیم که اسکن و نمایش توسط سونوگرافی سه بعدی، راههای بهتری برای بیمارانی با مشکلاتی همچون سرطان، تومور و پیوند ایجاد کردهاست.
تصویربرداری از عروق
حرکت عروق خونی و شریانها به دلیل توزیعشان به راحتی قابل رهگیری نیستند و در نتیجه گرفتن یک تصویر بیدرنگ از آنها مشکل است. تشخیص بهطور گسترده در هر نوع درمانی استفاده میشود و با سونوگرافی سه بعدی، اکنون حرکت دینامیکی مولکولهای خونی، وریدها و شریانها قابل رهگیری است.[12] علاوه بر این، انواع مختلفی از تشخیص مانند اندازهگیری قطر دیوار بین شریانها میتواند با یک ردیاب مجتمع در سونوگرافی سه بعدی که به مکانیابی دقیق کمک میکند شناسایی شود.[13] به این صورت این تکنولوژی به جراح کمک تصویری کرده و به علاوه، دارای یک سنسور است که به ردگیری محل عروق تحت جراحی کمک میکند.
بیهوشی موضعی
سونوگرافی سه بعدی بلا درنگ، در مرحله انسداد عصب پیرامونی، برای شناسایی آناتومی مرتبط و مانیتور پخش شدن بیهوشی موضعی در اطراف عصب کاربرد دارد. انسداد عصب پیرامونی مانع از انتقال سیگنالهای درد از مکان آسیب دیده به مغز بدون استفاده از بیهوشی شده که آن را برای استفاده در درمان سرپایی بیمارن ارتوپدی مناسب میکند. سونوگرافی سه بعدی بیدرنگ تشخیص عضلات، اعصاب و عروق را هنگامی که یک سوزن یا کاتتر به زیر پوست وارد میشود را ممکن میسازد. سونوگرافی سه بعدی قادر به نمایش سوزن بدون توجه به صحفهٔ تصویر، که یک پیشرفت قابل توجه نسبت به اولتراسوند دو بعدی است را ممکن میسازد. به علاوه، میتوان تصویر را در حالت بیدرنگ چرخاند یا برش داد تا ساختارهای آناتومی درون یک حجم از بافت مشخص شوند. پزشکان در کلینیک Mayo در Jacksonville در حال تحقیق بر روی روشی با استفاده از سونوگرافی سه بعدی بیدرنگ برای هدایت بیهوشی موضعی در جراحی شانه، مچ پا و زانو هستند.[14][15]
منابع
- Hoskins, Peter; Martin, Kevin; Thrush, Abigail (2010). Diagnostic ultrasound: physics and equipment (2nd ed.). Cambridge, UK: Cambridge University Press. ISBN 978-0-521-75710-2.
- Health, Center for Devices and Radiological. "Medical Imaging - Ultrasound Imaging". www.fda.gov.
- Baba, Kazunori; Okai, Takashi; Kozuma, Shiro; Taketani, Yuji (1999). "Fetal Abnormalities: Evaluation with Real-time-Processible Three-dimensional US—Preliminary Report". Radiology. 211 (2): 441–446. doi:10.1148/radiology.211.2.r99mr02441. PMID 10228526.
- Acar, Philippe; Battle, Laia; Dulac, Yves; Peyre, Marianne; Dubourdieu, Hélène; Hascoet, Sébastien; Groussolles, Marion; Vayssière, Christophe (2014). "Real-time three-dimensional foetal echocardiography using a new transabdominal xMATRIX array transducer". Archives of Cardiovascular Diseases. 107 (1): 4–9. doi:10.1016/j.acvd.2013.10.003. PMID 24364911.
- Huang, Qinghua; Zeng, Zhaozheng (2017). "A Review on Real-Time 3D Ultrasound Imaging Technology". BioMed Research International. 2017: 1–20. doi:10.1155/2017/6027029. PMC 5385255. PMID 28459067.
- Pedrosa, J.; Barbosa, D.; Almeida, N.; Bernard, O.; Bosch, J.; d'Hooge, J. (2016). "Cardiac Chamber Volumetric Assessment Using 3D Ultrasound - A Review". Current Pharmaceutical Design. 22 (1): 105–21. PMID 26548305.
- Picano, E.; Pellikka, P. A. (2013). "Stress echo applications beyond coronary artery disease". European Heart Journal. 35 (16): 1033–1040. doi:10.1093/eurheartj/eht350. PMID 24126880.
- Yan, P. (2016). "SU-F-T-41: 3D MTP-TRUS for Prostate Implant". Medical Physics. 43 (6Part13): 3470–3471. doi:10.1118/1.4956176.
- Ding, Mingyue; Cardinal, H. Neale; Fenster, Aaron (2003). "Automatic needle segmentation in three-dimensional ultrasound images using two orthogonal two-dimensional image projections". Medical Physics. 30 (2): 222–234. doi:10.1118/1.1538231. PMID 12607840.
- Mahboob, Syed; McPhillips, Rachael; Qiu, Zhen; Jiang, Yun; Meggs, Carl; Schiavone, Giuseppe; Button, Tim; Desmulliez, Marc; Demore, Christine (2016). "Intraoperative Ultrasound-Guided Resection of Gliomas: A Meta-Analysis and Review of the Literature". World Neurosurgery. 92: 255–263. doi:10.1016/j.wneu.2016.05.007. PMID 27178235.
- Moiyadi, Aliasgar V.; Shetty, Prakash (2016). "Direct navigated 3D ultrasound for resection of brain tumors: A useful tool for intraoperative image guidance". Neurosurgical Focus. 40 (3): E5. doi:10.3171/2015.12.FOCUS15529. PMID 26926063.
- Jin, Chang-zhu; Nam, Kweon-Ho; Paeng, Dong-Guk (2014). "The spatio-temporal variation of rat carotid artery bifurcation by ultrasound imaging". 2014 IEEE International Ultrasonics Symposium. pp. 1900–1903. doi:10.1109/ULTSYM.2014.0472. ISBN 978-1-4799-7049-0.
- Pfister, Karin; Schierling, Wilma; Jung, Ernst Michael; Apfelbeck, Hanna; Hennersperger, Christoph; Kasprzak, Piotr M. (2016). "Standardized 2D ultrasound versus 3D/4D ultrasound and image fusion for measurement of aortic aneurysm diameter in follow-up after EVAR". Clinical Hemorheology and Microcirculation. 62 (3): 249–260. doi:10.3233/CH-152012. PMID 26484714.
- "Real-Time 3-D Ultrasound Speeds Patient Recovery" (Press release). Mayo Clinic. July 13, 2007. Retrieved May 21, 2014.
- Feinglass, Neil G.; Clendenen, Steven R.; Torp, Klaus D.; Wang, R Doris; Castello, Ramon; Greengrass, Roy A. (2007). "Real-Time Three-Dimensional Ultrasound for Continuous Popliteal Blockade: A Case Report and Image Description". Anesthesia & Analgesia. 105 (1): 272–274. doi:10.1213/01.ane.0000265439.02497.a7. PMID 17578987.
پیوند به بیرون
- The History of Ultrasounds (including 3D ultrasounds)
- The Endowment for Human Development provides numerous 4D ultrasounds that can be viewed online.
- Scans uncover secrets of the womb BBC News
- About the discovery of medical ultrasonography
- Learn how to perform 3D/4d Ultrasounds
- Safety Concerns Details a number of health concerns over this unregulated practice
- 3D Ultrasound Clinic and Education Facility A 3D Ultrasound clinic in Sacramento, CA that specializes in performing 3D ultrasound and training sonographers.
