گالیم آرسنید
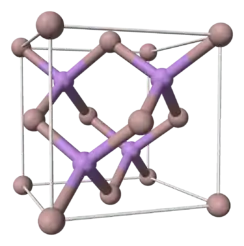
گالیم آرسنید(GaAs) یک ترکیب از عناصر گالیم و آرسنیکاست. این ترکیب یک نیمه هادی بوده و ساختار بلوری آن مشابه سولفید روی است.
| گالیم آرسنید | |
|---|---|
 | |
 | |
Preferred IUPAC name Gallium arsenide | |
| شناساگرها | |
| شماره ثبت سیایاس | 1303-00-0 |
| پابکم | 14770 |
| کماسپایدر | 14087 |
| شمارهٔ ئیسی | 215-114-8 |
| شمارهٔ یواِن | 1557 |
| MeSH | gallium+arsenide |
| شمارهٔ آرتیئیسیاس | LW8800000 |
| جیمول-تصاویر سه بعدی | Image 1 |
SMILES
| |
| |
| خصوصیات | |
| فرمول مولکولی | GaAs |
| جرم مولی | 144.645 g/mol |
| شکل ظاهری | Very dark red vitreous crystals |
| بوی | garlic-like when moistened |
| چگالی | 5.3176 g/cm3 |
| دمای ذوب | ۱٬۲۳۸ درجه سلسیوس (۲٬۲۶۰ درجه فارنهایت؛ ۱٬۵۱۱ کلوین) |
| انحلالپذیری در آب | insoluble |
| انحلالپذیری | soluble in HCL insoluble in ethanol methanol acetone |
| نوار ممنوعه | 1.424 eV (at 300 K) |
| تحرکپذیری | 8500 cm2/(V·s) (at 300 K) |
| رسانندگی گرمایی | 0.55 W/(cm·K) (at 300 K) |
| ضریب شکست (nD) | 3.8[1] |
| ساختار | |
| ساختار بلوری | Zinc blende |
| گروه فضایی | T2d-F-43m |
| ثابت شبکه | a = 565.35 pm |
| Tetrahedral | |
| شکل مولکولی | Linear |
| خطرات | |
| GHS pictograms |   |
| سیستم هماهنگ جهانی طبقهبندی و برچسبگذاری مواد شیمیایی | DANGER |
| GHS hazard statements | H301, H331, H410 |
| GHS precautionary statements | P261, P273, P301+310, P311, P501 |
| لوزی آتش | |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
گالیم آرسنید در تولید دستگاههای مانند مایکروویو ،دیودهای ساطعکننده نور مادون قرمز، دیود های لیزر و سلولهای خورشیدی استفاده میشود.
گالیم آرسنید اغلب به عنوان یک ماده بستر برای رشد رونشستی (epitaxial growth ) در دیگر نیمه هادیهای III-V semiconductors شامل ایدیم گالیم آرسناید( indium gallium arsenide)، آلومینیوم گالیم آرسناید ( aluminum gallium arsenide ) و بقیه استفاده میشود.
آمادهسازی و شیمی
در این ترکیب، گالیم دارای غدد اکسیداسیون 3+است.تک کریستال های گالیم آرسنید را میتوان توسط نوع سه فرآیند صنعتی تولید کرد:[2]
- فرآیندیخ زدگی با افت حرارت عمودی (VGF) (اکثر ویفرهای گالیم آرسنید با استفاده از این فرایند تولید میشوند).[3]
- رشد بلور با استفاده از یک کوره افقی و با استفاده از روش Bridgman-Stockbarger که در آن بخارات گالیم و آرسنیک واکنش نشان میدهند و مولکولهای آزاد شده در یک دانه کریستال در خنککنندهای که در انتهای کوره قرار دارد تهنشین میشوند.
- روش رشد مایع محصور (فرایند چکرالسکی) برای تولید با خلوص بالا تک کریستالها است.
روشهای جایگزین برای تولید صفحه گالیم آرسنید عبارتند از:[4]
- (VPE) واکنش گازی فلز گالیم و آرسنیک تری کلرید: 2 Ga + 2 AsCl 3 → 2 GaAs + 3 Cl 2
- ( برآرایی بخار فلز-آلی) واکنش تری متیل گالیم و آرسنیک: 4 Ga + As4 → 4 GaAs یا 2 Ga + As2 → 2 GaAs
اکسیداسیون گالیم آرسنیددر هوا رخ میدهد عملکرد این نیمه هادی را پایین میآورد. برای مقاوم کردن سطح ماده میتوان یک لایه گالیم(II) سولفید بر روی آن با استفاده از یکی از ترکیبات tert-بوتیل گالیم سولفید تهنشین کرد .[5]
_2%22_wafer.jpg.webp)
نیمه عایق کریستال
اگر یک کریستال گالیم آرسنید در حضور مقدار زیادی آرسنیک رشد کند, در آن برخی از نقص ها به وجود میآید،به ویژه نقوص anti-site آرسنیک (یک اتم آرسنیک درجای یک اتم گالیم در شبکه بلور). خواص الکترونیکی این نقوص (در تعامل با دیگران) باعث میشود که سطح فرمی به نزدیکی مرکز نوار ممنوعه متصل شود، بهطوری که کریستال گالیم آرسنید دارای غلظت بسیار کم الکترون و حفره شود. این غلظت حامل پایین شبیه به کریستال طبیعی است, اما در عمل رسیدن به آن بسیار سادهتر است. این کریستالها "نیمه عایق" نام دارند،که مقاومت بالای 107-109 Ω·سانتی متر را دارا میباشند (که بسیار بالا برای یک نیمه هادی است, اما هنوز هم بسیار پایینتر از یک عایق واقعی مانند شیشه است).[6]
قلم زنی
قلم زنی خیس گالیم آرسنید به صورت صنعتی با استفاده از یک عامل اکسیدکننده مانند آب اکسیژنه یا آب برم[7] انجام میشود، و همان استراتژی قبلی در ثبت اختراع مربوط به پردازش ضایعات قطعات حاوی گالیم آرسنید که در آن Ga3+
با اسید هیدروکسام("HA")مخلوط میشود استفاده میشود. برای مثال:[8]
- GaAs + H2O2 + "HA" → "GaA" + H3AsO4 + H2O4
این واکنش آرسنیک اسید تولید میکند.
الکترونیک
گالیم آرسنید منطق دیجیتال
گالیم آرسنید میتواند برای انواع زیادی ترانزیستور استفاده شود:[9]
- MESFET
- HEMT (یک نوع FET)
- JFET
- ترانزیستور پیوند نامتناجس (HBT)
- (VeladiFET (VFET
HBT میتواند در منطق تزریق یکپارچه استفاده شود. اولین گیتهای منطقی گالیم آرسنید از منطق بافر(FET) استفاده میکردند.
از ~1975 تا 1995 خانوادههای اصلی منطق مورد استفاده عبارت بودند از:
- منطق منبع-همراه (FET) (SCFL) سریعترین و پیچیدهترین کار (مورد استفاده توسط TriQuint و Vitesse)
- منطق خازن دیود (FET) (CDFL) (مورد استفاده توسط Cray)
- منطق مستقیم همراه (FET) (DCFL) سادهترین و کمترین قدرت (مورد استفاده توسط Vitesse برای VSLI دروازه آرایه ها)
مقایسه با سیلیکون در الکترونیک
مزایای گالیم آرسنید
برخی از خواص الکترونی گالیم آرسنید نسبت به سیلیکون برتر هستند. گالیم آرسنید سرعت اشباع الکترون بالاتر و تحرکپذیری بالاتری دارد،که اجازه میدهد ترانزیستورهای گالیم آرسنید در فرکانسهای بیش از 250 GHz نیز عملکرد خوبی داشته باشند. دستگاههای گالیم آرسنید نسبتا غیر حساس به حرارت بالا، با توجه به انرژی منطقه ممنوعه گسترده تر، و آنها نیز تمایل به ایجاد نویز کمتری در مدارهای الکترونیکی نسبت به دستگاههای سیلیکون به خصوص در فرکانسهای بالا دارند.این ویژگیهای برتر گالیم آرسنید دلایل قانعکنندهای برای استفاده از GaAs در مدارات گوشیهای موبایل،ارتباطات ماهواره ای، مایکروویو لینکهای نقطه به نقطه و سیستم های رادار با فرکانس بالاتر است. گالیم آرسنید همچنین در ساخت دیود گان برای نسل مایکروویو استفاده میشود .
یکی دیگر از مزایای استفاده از گالیم آرسنید این است که آن گاف مستقيم دارد, که بدان معنی است که گالیم آرسنید میتواند برای جذب و تابش نور به صورت مؤثر استفاده شود. سیلیکون گاف غيرمستقيم داردو بنابراین در ساطع کردن نور نسبتا ضعیف است.
به عنوان گستردهای مستقیم گاف مواد با نتیجه مقاومت به تابش آسیب GaAs یک ماده بسیار عالی برای فضای بیرونی الکترونیک نوری و ویندوز در قدرت بالا برنامههای کاربردی.
مزایای سیلیکون
سیلیکون دارای سه مزیت عمده نسبتبه گالیم آرسنید در ساخت مدار مجتمع است . نخست، سیلیکون فراوان است وفرآیند تبدیل به شکل مواد معدنیسیلیکات برای آن ارزان است.
در ضمن یک کریستال سیلیکون دارای ساختار بسیار پایدار است و کریستال آن میتواند تا قطر بسیار بزرگ رشد کندو پردازش آن عملکرد بسیار خوبی را دارا است. سیلیکون نیز هادی نسبتا خوب حرارتی است، بنابراین امکان متراکمسازی و بستهبندی ترانزیستورهایی که نیاز به خلاص شدن از گرمای خود را دارند فراهم میکند، بنابراین بسیار مطلوب برای طراحی و ساخت Ic های بسیار بزرگ میباشند . چنین ویژگیهای خوب مکانیکی نیز آن را به ماده مناسب برای زمینه در حال توسعه نانو تبدیل کردهاست. بهطور طبیعی, سطح گالیم آرسنید نمیتواند در برابر دمای بالا مورد نیاز برای نفوذ مقاومت کند.[10]
دومین مزیت عمدهٔ سیلیکون وجود یک اکسید بومی (دی اکسید سیلیکونبا SiO2) است،که به عنوان یک عایق در دستگاههای الکترونیکی استفاده شدهاست . دیاکسید سیلیکون به راحتی میتواند بر روی مدار سیلیکون گنجانیده شده و این چنین لایههایی لایههای چسبنده به زمینهٔ سیلیکون هستند. SiO2 نه تنها عایق خوبی است(با یک گاف از 8.9 eV)، بلکه سطح Si-SiO2 به راحتی میتواند مهندسی شود تا به خواص الکتریکی عالی برسد. گالیم آرسنید اکسید بومی ندارد، به راحتی لایه عایق پایدار چسبنده را پشتیبانی نمیکند و دارای قدرت دی الکتریک یا خواص رویینگی سطح سیلیکون یا سیلیکون دیاکسید نیست.
سوم مزیت سیلیکون آن است که سیلیکون دارای سوراخ تحرک بالاتر در مقایسه با گالیم آرسنید (500 مقابل 400 سانتی متر2V-1s-1)است.[11] این تحرک بالا اجازه میدهد که سرعت ساخت ترانزیستور اثر میدان (FET) بالاتر رود ،که مورد نیاز برای منطق CMOS است.
منابع
- Refractive index of GaAs. Ioffe database
- Moss, S. J.; Ledwith, A. (1987). The Chemistry of the Semiconductor Industry. Springer. ISBN 0-216-92005-1.
- Scheel, Hans J.; Tsuguo Fukuda. (2003). Crystal Growth Technology. Wiley. ISBN 0471490598.
- Smart, Lesley; Moore, Elaine A. (2005). Solid State Chemistry: An Introduction. CRC Press. ISBN 0-7487-7516-1.
- "Chemical vapor deposition from single organometallic precursors" A. R. Barron, M. B. Power, A. N. MacInnes, A. F.Hepp, P. P. Jenkins U.S. Patent ۵٬۳۰۰٬۳۲۰ (1994)
- McCluskey, Matthew D. and Haller, Eugene E. (2012) Dopants and Defects in Semiconductors, pp. 41 and 66, شابک ۹۷۸−۱۴۳۹۸۳۱۵۲۶
- Brozel, M. R.; Stillman, G. E. (1996). Properties of Gallium Arsenide. IEEE Inspec. ISBN 0-85296-885-X.
- "Oxidative dissolution of gallium arsenide and separation of gallium from arsenic" J. P. Coleman and B. F. Monzyk U.S. Patent ۴٬۷۵۹٬۹۱۷ (1988)
- Dennis Fisher; I. J. Bahl (1995). Gallium Arsenide IC Applications Handbook. 1. Elsevier. p. 61. ISBN 978-0-12-257735-2. 'Clear search' to see pages
- Morgan, D. V.; Board, K. (1991). An Introduction To Semiconductor Microtechnology (2nd ed.). Chichester, West Sussex, England: John Wiley & Sons. p. 137. ISBN 0471924784.
- Appendix G, Sze, S. M. (1985). Semiconductor Devices Physics and Technology, John Wiley & Sons شابک ۰−۴۷۱−۸۷۴۲۴−۸
