نظریه جنبشی
نظریه جنبشیمولکولی گازها یا به اختصارنظریه جنبشی (به انگلیسی: Kinetic theory) از مهمترین نظریههای ترمودینامیک است که در آن به بحث دربارهٔ تغییر موقعیت ذرات و حرکت آنها در اثر تغییر پارامترهایی مثل حجم و فشار میپردازند. نظریه جنبشی را شیمیدانها و فیزیکدانهای مختلف به مرور زمان گسترش دادهاند و در حال حاضر همهٔ حالتهای ماده از جمله گاز، مایع، جامد و پلاسما مورد بحث در این نظریه است.
| مکانیک آماری |
|---|
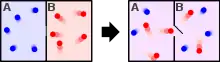 |
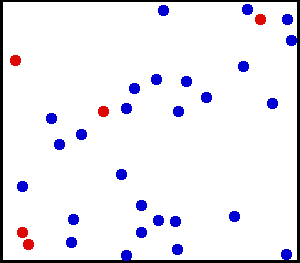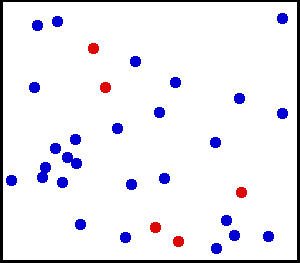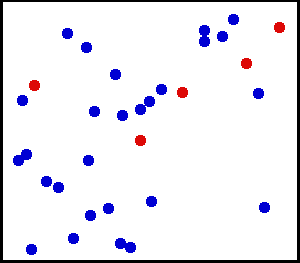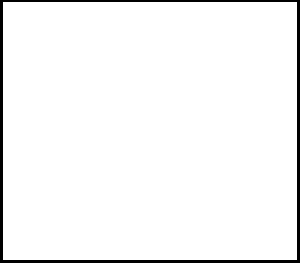
حرکت مولکولی
حرکت مولکولی از موضوعات مورد بحث در تئوری سینماتیک مولکولی است. زمانی که دما یا فشار سیستم تغییر میکند حرکت مولکولها نیز به تبع آن دچار تغییر میشود. این تغییر حرکت میتواند شامل حرکتهای چرخشی و ارتعاشی در جامدات و نیز حرکت انتقالی چرخشی و ارتعاشی در مایعات و گازها باشد. با در نظر گرفتن تغییر حرکت مولکولها نسبت به زمان میتوان سرعت این تغییرات را تعیین کرد.
1- حرکت انتقالی: یعنی از جایی به جای دیگر رفتن : در این حالت مولکول ها کمترین انرژی را به خود می گیرند. و در جریان های همرفتی ،مواد به این طریق انرژی را انتقال می دهند. و در دو حالت مواد یعنی مایع و گاز صورت می گیرد.
2-حرکت ارتعاشی : این حرکت می تواند در هر سه حالت ماده روی دهد و باعث انجام بسیاری از پدیده ها مانند انبساط و انتقال گرما از طریق رسانش شود و مواد گرمایی را که به این طریق جذب می کنند می توانند مجددا تابش کنند که این تابش همان اشعه فروسرخ است.
3-حرکت چرخشی: این انرژی در گازها و مایعات وجود دارد و جالب این است که این حرکت در آب وجود ندارد و مولکول های آب قادر نیستند که حرکت چرخشی از خود انجام دهند مگر اینکه دمای آب به حدود 42 درجه سانتی گراد برسد که در این دما مولکول ها با سرعت بسیار زیاد به دور خود می چرخند و باعث گسستگی پیوندهای بین مولکولی می شوند و چون 40% بدن انسان و 90% بدن موجودات زنده را آب تشکیل می دهد و دقیقا در این دما مرگ آدمی فرا می رسد و بهطور کلی روندهای حیاتی خود را از فاصله دمایی 42 تا 45 درجه دور نگه می دارند.
منابع
- Kinetic Theory of Gases- by Stephen G. Brush and Nancy S. Hall- Imperial college press- 2003
