عیوب نقطهای
عیوب نقطهای (به انگلیسی: Point Defects) به دستهای از ناکاملیهای بلوری گفته میشود که بسته به ماهیتشان منجر به وجود آمدن نقص در تعداد متناهی و کوچک اتم در شبکه بلوری میشوند. این تعداد مستقل از اندازهٔ بلور و ریزساختار ماده است.
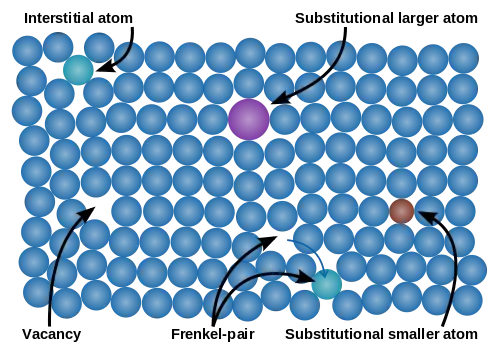
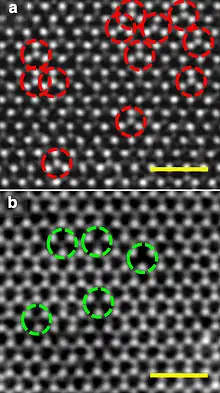
معمولاً از نشانهگذاری کروگر-وینک برای نمایش عیوب نقطهای استفاده میشود. این عیوب را میتوان با استفاده از روشهایی مشاهده کرد . از جمله این روشها استفاده از میکروسکوپ الکترونی عبوری TEM است.
عیب جای خالی یا تهی جایی (Vacancy)
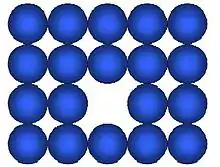
تهیجایی زمانی اتفاق می افتد که اتمی در جای خود در شبکه بلوری وجود نداشته باشد . بهطور مثال فقط در 7 گوشه از 8 گوشه یک مکعب، اتم وجود داشته باشد و جای یکی از آنها در گوشه مکعب خالی باشد به این ترتیب این مکعب یک جای خالی دارد.این عیب سادهترین و در عین حال رایجترین عیوب سطحی است . چنین عیوبی میتواند در موقع انجماد تغییر شکل دادن،اشعه دادن با انرژی زیاد ویا در درجه حرارتهای بالا به وجود بیاید، وجود نقص جای خالی منجر به نزدیک شدن اتمهای اطراف جای خالی میشود که این امر تنش کششی را میان اتمهای مجاور جای خالی به وجود میآورد و لذا نظم اتمی به هم میریزد.
در یک جسم در حالت تعادل همیشه تعدادی جای خالی وجود دارد که تعداد آنها رابطه مستقیمی با درجه حرارت دارد. بنابراین با افزایش یا کاهش دما میتوان تعداد جاهای خالی را در ساختار کریستال تغییر داد. لزوم حضور جاهای خالی را نیز با استفاده از اصول ترمودینامیک میتوان اثبات نمود و تنها این عیوب هستند که در حالت حرارتی به وجود می آیند و بقییه عیوب کریستالی از نظر ترمودینامیکی در تعادل نیست و در اثر عوامل خارجی به وجود می آیند.
تعداد تعادلی جاهای خالی برای مقدار معینی از ماده ،وابسته به دما بوده و طبق رابطه زیر با دما افزایش می یابد:
در عبارت فوق ،Nکل تعداد مکانهای اتمی ،Qν انرژی لازم برای یک جاخالی،Tدمای مطلق بر حسب کلوین و k ثابت گازها یا ثابت بولتزمن است(مقدار k برابر است)[1]
عیب بین نشینی (interstitial)
بین نشینی قرار گرفتن اتمی اضافی در فضای خالی بین اتمهای دیگر از ساختار کریستالی است که معمولاً باعث اعوجاج و بی نظمی در ساختار کریستالی میشود . این اتمها میتوانند از جنس اتمهای ساختار کریستالی باشند که به صورت اتمی اضافی در ساختار نمود پیدا کردهاست یا به صورت ناخالصی حل شده باشند . اتمها ی بیننشین معمولاً در حفراتی که در ساختار کریستالی وجود دارند قرار میگیرند و برای این منظور اغلب شعاع اتمی کمتری از اتمهای اصلی موجود در ساختار دارند.
این اتم اضافی موجب ایجاد تنش فشاری در ساختار اتم میگردد و در نتیجه موجب افزایش انرژی در آن نقطه میشود.
عیب جانشینی ( Substitutional )
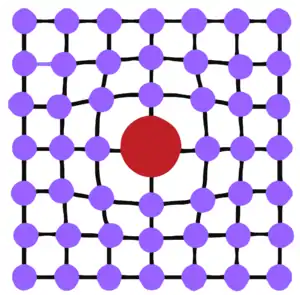
عیب جا نشینی زمانی رخ میدهد که اتم حل شونده جایگزین یکی از اتمهای شبکه بلور گردد. چون اندازه شعاع اتمی اتم حل شونده با اتم شبکه بلور متفاوت است، جانشینی موجب بی نظمی و خمیدگی در ساختار شبکه بلور میشود .اگر اندازه شعاع اتمی اتم جانشین شده کوچکتر از اتمهای موجود در ساختار بلور باشد تنش کششی و در صورت بزرگتر بودن اندازه شعاع اتمی اتم جانشین شده، تنش فشاری خواهد بود.
نا کاملی بلور ی در فلزات (Imperfections in metals)
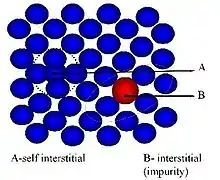
در فلزات بسته به شرایط تمامی عیوب تهی جایی، بین نشینی و جانشینی امکان وقوع دارند .در فلزات خالص نقص جای خالی یا خود بین نشینی( self – interstitial ) رخ میدهد، خود بین نشینی از جابجایی یک اتم خودی در شبکه بلور ایجاد میشود که با این جابجایی در قسمتی دیگر از کریستال تهی جایی ایجاد میشود . با اضافه کردن ناخالصی به فلز بسته به نسبت اندازه شعاع اتمی اتم حل شونده و شبکه بلور میتوان انتظار داشت عیوب بین نشینی یا جانشینی اتفاق افتد . به عنوان مثال با اضافه کردن کربن به آهن، به علت کوچک بودن اندازه شعاع اتمی کربن در مثایسه با آهن، کربن میتواند در فضاهای خالی بین اتمهای آهن قرار گیرد و به این ترتیب بین نشینی رخ دهد . در مقابل با اضافه کردن مس به بلور نیکل به علت اختلاف کمنر میان شعاغ اتمی آن دو شاهد جانشینی خواهیم بود.
جانشینی و حل شدن جامدات در فلزات تحت شرایط خاصی رخ میدهد که از آن شرایط تحت عنوان قوانین هیوم-روتری یاد میشود .
این شرایط عبارت است از :
1- تفاوت شعاع اتمی حل شونده و اتمهای موجود در شبکه کمتر از 15 درصد شعاع اتمی آنها باشد.
2- اتمهای حلال و حل شونده دارای الکترونگاتیوی مشابه باشند.
3- ساختار کریستالی فلزات خالص هر دو ماده شبیه یکدیگر باشند.
4- دو ماده دارای الکترونهای ظرفیت یکسانd باشند یا در صورت متفاوت بودن، فلزات تمایل بیشتری برای حل کردن فلز دیگری با ظرفیت الکترونی بیشتر دارد.
در محلولهای جامد بین نشینی ،اتمهای ناخالصی حفرهها یا مکانهای بین نشینی موجود در بین اتمهای میزبان را پر میکنند.برای مواد فلزی که دارای فاکتور تراکم اتمی بالا هستند،این موقعیتهای بین نشینی نسبتا کوچک میباشند. در نتیجه ،قطر اتمی یک ناخالص بین نشینی باید به اندازه کافی کوچکتر ازقطر اتمهای میزبان باشد.[1]
ناکاملی بلوری در سرامیکها (Imperfections in Ceramics)
سرامیکها داری ساختار یونی هستند . بنابراین باید در تمامی قسمتهای بلور سرامیکها شرایط الکتروخنثایی در نظر گرفته شود. در سرامیکها مانند فلزات نقص تهی جایی میتواند به وجود آید. یعنی در شبکه بلور سرامیکها ممکن است به جای کاتیون یا آنیون حفره باشد.این عیب زمانی میتواند به وجود آید که آنیون یا کاتیونی بین نشینی نیز در سرامیکها مشاهده میشود .بین نشینی در سرامیکها با جابحایی یکی از کاتیونها و قرارگیری آن در یک موقغیت بین نشینی رخ میدهد و به این صورت در یک نقطه شاهد تراکم کاتیون و در نقطه دیگر شاهد جای خالی در بلور سرامیک خواهیم بود .
بر این اساس در سرامیکها دو عیب دیگر را نیز میتوان طبثه بندی کرد .
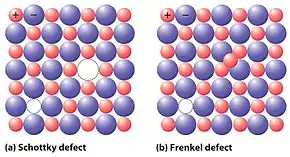
عیب شاتکی (Schottky defect)
اگر در ساختار شبکه بلور یک سرامیک همزمان با یکدیگر یک کاتیون و آنیون موجود نباشد، در آن ساختار عیب شاتکی خواهیم داشت عیب شاتکی میتواند بدین طریق به وجود بیاید که یک اتم باردار شبکه به وسیله یک اتم با بار(ظرفیت) کمتر یا بیشتر جایگزین شود.
تعداد تعادلی عیوب شاتکی از رابطه زیر به دست می اید:[1]
Qsانرژی لازم برای تشکیل هر عیب شاتکی،kوTنیز ثابت بولتزمن و دمای مطلق میباشند.
عیب فرنکل (Frenkel defect)
عیب فرنکل زمانی به وجود میآید که یک کاتیون از موقعیت خود به یک موقعیت بین نشینی برود .در شرایط عادی یک آنیون به علت اندازه بزرگتر در مقایسه با کاتیون، به هیچ عنوان نمیتواند از موقعیت خود به یک موقعیت بین نشینی نقل مکان کند و موجب عیب فرنکل گردد .
همچنین تعداد تعادلی عیوب فرنکل همانند عیب شاتکی از رابطه زیر بدست می اید:[1]
کاربرد ها

ایجاد و کنترل عیوب نقطهای کاربردهای ویژهای در ساخت مواد و آلیاژهایی با ویژگیهای خاص و قابل کنترل دارد. پل ارتباطی بین عیوب نقطهای و این کاربردهای صنعتی پدیده نفوذ است. که یکی از مهمترین عوامل ایجاد پدیده نفوذ در جامدات، عیب تهیجایی است. در ساحتارهای سرامیکی یونی عیوب فرنکل و شاتکی نقش به سزایی در ایجاد مواد با کاربردهای گسترده الکترونیکی ایفا میکند. بدین صورت که میتوان با افزودن موادی ( به عنوان مثال فسفر . یا آلومینیوم) و ورود آنها به ساختار کریستالی این سرامیکها و جایگیری مناسب آنها در حفرات و فضاهای خالی ناشی از عیوب فرنکل و شاتکی در ساخت ترانزیستورها و نیمه هادی هاو ساختار P-N-P یا N-P-N از آنها بهره برد
جستارهای وابسته
منابع
- Callister, William D., and David G. Rethwisch (۲۰۰۸). Fundamentals of Materials Science and Engineering: An Integrated Approach. John Wiley & Sons,.
- Callister, William D., and David G. Rethwisch. Fundamentals of Materials Science and Engineering: An Integrated Approach. Hoboken, NJ: John Wiley & Sons, 2008.
- Foundations of Materials Science and Engineering ,5TH EDITION,William Smith and Javad Hashemi.
- A kelly, G.W. Groves- Crystallography and crystall defects - Addison-Wesley-1970
- Efthimios Kaxiras, Atomic and Electronic Structure of Solids, Cambrdge University Press, 2003. ISBN 978-0-521-81010-4
- The role of ionic point defects in the catalytic activity of ionic crystals. George Simkovich, Carl Wagner.
