واکنش جانشینی هستهدوستی دومولکولی
واکنش جانشینی هسته دوست دو مولکولی (به انگلیسی: bimolecular nucleophilic substitution) که به اختصار SN۲ نیز شناخته میشود، گونهای از واکنشهای جانشینی هسته دوست در واکنشهای آلی است. دسته دیگری از واکنشهای استخلافی وجود دارند که در آنها گروه ترککننده همزمان با حمله گونه هستهدوست مجبور به ترک مولکول میشود. این دست از واکنشها را واکنشهای استخلافی هسته دوستی از نوع درجه دوم یا دومولکولی (SN2) گویند که در یک مرحله انجام میشوند. همانگونه که از نام واکنش پیداست، سرعت واکنش از نوع درجه دوم یا دومولکولی میباشد، بدین معنی که در مرحله تعیینکننده سرعت دو مولکول در معادله سرعت وارد میشوند و سرعت بستگی به غلظت هر دو گونه دارد. سرعت در این دست از واکنشها تحت تأثیر نوع هسته دوست، نوع جزء مورد عمل (نوع آلکیل)، ترککننده و حلال میباشد. همان گونه که اشاره شد واکنش SN2 برخلاف SN1، فقط در یک مرحله رخ میدهد. این واکنشها همچنین باعث وارونگی آرایش فضایی کربن حامل گروه ترککننده میگردد. زیرا در واکنشهای SN2، هستهدوست همیشه از پشت به جزء مورد عمل حمله میکند و گروه ترک-کننده مجبور به ترک از سمت مخالف میشود. این وارونگی را میتوان توسط ترکیبهای فعال نوری مشاهده کرد.
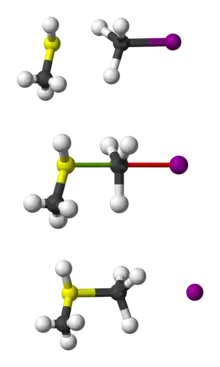
عوامل مؤثر بر واکنش جانشینی هسته دوست دو مولکولی
قدرت هستهدوست
یکی از عوامل مهم تعیینکننده مسیر واکنشهای استخلافی، قدرت هستهدوست میباشد. عوامل مختلفی از جمله حلال، قطبشپذیری و قدرت بازی بر قدرت هستهدوست اثر دارند. بهطورکلی با افزایش قدرت بازی، قدرت هستهدوستی نیز افزایش مییابد. عناصر با شعاع اتمی بیشتر (اتمهای بزرگتر) پراکندگی ابر الکترونی بیشتر و در نتیجه قطبشپذیرتراند. این امر سبب میشود امکان همپوشانی بهتر و مؤثرتر اوربیتالها در حالتگذار فراهم گردد، در نتیجه انرژی حالتگذار کاهش یافته و واکنش سریعتر پیش میرود.
حلال
حلال مناسب برای واکنش SN2 حلال آپرتیک (بدون پروتون) قطبی میباشد. حلالهای آپرتیک کانیون هارا حلال پوشی میکنند و از سرعت آن میکاهند. پدیده مهم دیگر که بر قدرت و فعالیت هستهدوست تأثیرگذار است، حلال و میزان حلالپوشی هستهدوست میباشد. وقتی یک جامد حل میشود، ذرات سازنده ساختار آن توسط حلال احاطه میگردند و نیروهای بین ذرات سازنده جسم جامد با نیروهای تازهای که حاصل برهمکنش حلال و ذرات سازنده جسم جامد است، جایگزین میگردد. این پدیده را حلالپوشی گویند. حلالپوشی معمولاً قدرت هستهدوستی را کاهش میدهد.
گروه ترککننده
هرچه گروه ترککننده متصل به کربن مرکزی، الکترونگاتیوتر باشد یا الکترون را راحتتر در اوربیتالهای خود جای دهد ترککننده مناسبتری خواهد بود.
ممانعت فضایی
واکنش SN2 بسیار به ممانعت فضایی حساس بوده (فضا ویژه) حمله از پشت به کربن انجام میشود و با معکوس شدن کانفیگوراسیون (صورتبندی) مولکول همراه است. یکی دیگر از عوامل مهم و تعیینکننده در واکنشهای استخلافی SN2، ساختار مولکول یا گروههای آلکیل در محل و اطراف جزء مورد عمل میباشد. کربنهایی که نمیتوانند بهراحتی به-صورت کربوکاتیون درآیند مانند کربنهای نوع اول، متیل و غیره واکنش استخلافی SN2انجام میدهند. طولانی شدن زنجیر و شاخهدار شدن کربن مجاور کربن محل واکنش نیز سرعت واکنش SN2 را کاهش میدهد. زیرا جایگزین کردن گروههای آلکیل در کربن حامل گروه ترککننده، منجر به ایجاد ممانعت فضایی میشود و این امر باعث کاهش سرعت واکنش میگردد[1]
جستارهای وابسته
منابع
- موریسون، رابرت تورنتون؛ بوید، نیلسون (۱۳۸۷). شیمی آلی. اول. ترجمهٔ علی سیدی اصفهانی، عیسی یاوری، احمد میرشکرایی. تهران: نشر علوم دانشگاهی. ص. ۲۱۷٬۲۱۸. شابک ۹۶۴-۶۱۸۶-۲۸-۹.
