دیبوران
| دیبوران | |
|---|---|
 | |
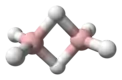 | |
(Diborane(6 | |
دیگر نامها Boroethane Boron hydride Diboron hexahydride | |
| شناساگرها | |
| شماره ثبت سیایاس | 19287-45-7 |
| کماسپایدر | 17215804 |
| شمارهٔ ئیسی | 242-940-6 |
| ChEBI | CHEBI:33590 |
| شمارهٔ آرتیئیسیاس | HQ9275000 |
| جیمول-تصاویر سه بعدی | Image 1 |
SMILES
| |
| |
| خصوصیات | |
| فرمول مولکولی | H6B2 |
| جرم مولی | ۲۷٫۶۷ g mol−1 |
| شکل ظاهری | Colorless gas |
| چگالی | 1.216 g/dm3 |
| دمای ذوب | −۱۶۴٫۸۵ درجه سلسیوس (−۲۶۴٫۷۳ درجه فارنهایت؛ ۱۰۸٫۳۰ کلوین) |
| دمای جوش | −۹۲٫۵ درجه سلسیوس (−۱۳۴٫۵ درجه فارنهایت؛ ۱۸۰٫۷ کلوین) |
| ساختار | |
| چهاروجهی (for boron) | |
| شکل مولکولی | see text |
| گشتاور دوقطبی | 0 D |
| خطرات | |
| لوزی آتش | |
| دمای خودآتشگیری | |
| ترکیبات مرتبط | |
| مرتبط با boron compounds | دکبوران تریفلورید بور |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
معرفی
دیبوران (به انگلیسی: Diborane) یک ترکیب شیمیایی است. شکل ظاهری این ترکیب، گاز بیرنگ و آتشزا و دارای بوی شیرین زننده است. ترکیب شیمیایی دی بوران حاوی بور و هیدروژن با فرمول شیمایی B2H6 است . دی بوران اسامی مختلفی دارد که شامل ،بورتان، بورن هیدرید، دی بورن هگزا هیدرید می باشند. دی بوران یک ترکیب کلیدی بور است که کاربرد های متنوع دارد . به دلیل ساختار الکترونی مورد توجه بسیاری قرار گرفته است.
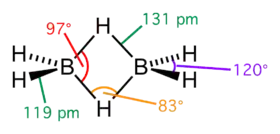
ساختار و پیوند
ساختار دی بوران دارای یک تقارن مولکولی است . چهار هیدرید پایانه هستند درحالی که دو پل بین مراکز بور وجود دارد. طول پیوند بور-پل هیدروژنی و طول پیوند بور-هیدروژن پایانه به ترتیب 1.33 و 1.19 آنگستروم است. به دلیل اختلاف در طول پیوند استحکام مکانیکی آنها نیز اختلاف دارند. پیوند بور-پل هیدروژنی ضعیف تر است. پیوند بین اتم های بور و اتم های هیدروژن پل زده متفاوت از مولکول های هیدروکربن است. هر اتم بور از دو الکترون در اتصال به اتم های هیدروژن پایانه استفاده میکند و یک الکترون ظرفیت باقی مانده برای اتصال اضافی دارد. اتم های هیدروژن پل زده هرکدام یک الکترون تامین میکنند. حلقه های دی بوران توسط چهار الکترون که دو پیوند ( 3 مرکز 2 الکترون ) نگهداشته شدند.
تولید و سنتز دی بوران
مطالعات در مورد دی بوران منجر به توسعه سنتز چندگانه شده است . سنتز صنعتی دی بوران شامل احیا تریفلورید بور توسط سدیم هیدرید، لیتیم هیدرید یا لیتیم آلومینیوم هیدرید انجام میشود. دو روش آزمایشگایی وجود دارد که شامل واکنش تریکلرید بور با لیتیم آلومینیوم هیدرید ، یا تریفلورید بور با سدیم تترا هیدروبورات است .
BCl3 + 3 LiAlH4 → 2 B2H6 + 3 LiAlCl
BF3 + 3 NaBH4 → 2 B2H6 + 3 NaBF4
کاربرد ها
دی بوران به عنوان پیشرانه موشکی مورد تست قرار گرفته است و احتراق به شدت گرما زا است . همچنین دی بوران به عنوان rubber vulcaniser ، به عنوان کاتالیست برای پلیمریزاسیون هیدروژن ، به عنوان شتاب دهنده سرعت شعله و همچنین برای پوشش دیواره توکامک ها برای کاهش میزان ناخالصی های فلزات سنگین در پلاسمای هسته استفاده می شود.

