انتروکوک فکالیس
انتروکوک فکالیس (Enterococcus faecalis) گونهای از انتروکوک است. پیشتر، این باکتری همراه با استرپتوکوکهای گروه D طبقهبندی میشد. انتروکوک فکالیس، باکتری همزیست روده انسان و سایر پستانداران است.[1] همچنین در برخی از مکملهای غذایی پروبیوتیکی نیز بکار میرود.[2] انتروکوک فکالیس در ایجاد عفونتهای بیمارستانی نقش دارد.[1] این باکتری بهطور ذاتی به بسیاری از آنتی بیوتیکها مقاوم است. انتروکوک فکالیس در کانال ریشه دندانهایی که تحت دستکاریهای دندانپزشکی قرار گفتهاند نیز بهطور گسترده دیده شدهاست.[3]
| انتروکوک فکالیس | |
|---|---|
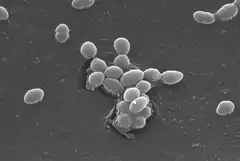 | |
| تصویر میکروسکوپ الکترونی از انتروکوک فکالیس | |
| آرایهشناسی | |
| فرمانرو: | باکتریها |
| شاخه: | فیرمیکوتس |
| رده: | باسیلها |
| راسته: | لاکتوباسیلالس |
| تیره: | انتروکوکاسیه |
| سرده: | انتروکوک |
| گونه: | انتروکوک فکالیس |
فیزیولوژی
انتروکوک فکالیس، غیر متحرک و بیهوازی اختیاری است. گلوکز را بدون ایجاد گاز تخمیر میکند و کاتالاز منفی است. اگر بر روی آگار خوندار رشد کند، واکنش کاتالاز مثبت کاذب است. این باکتری، شیر لیتموس را احیا کرده اما ژلاتین را مایع نمیکند.
بیماریزایی
انتروکوک فکالیس، بیماریهایی مانند اندوکاردیت، با کتریمی، عفونتهای ادراری و مننژیت در انسان ایجاد میکند. این باکتری دارای فاکتورهای بیماریزایی گوناگونی است.[4] نوعی همولیزین کد شده توسط پلاسمید به نام سیتولیزین، فاکتور بیماریزای مهمی در مدلهای حیوانی است. سیتولیزین به همراه مقاومت بالا به آنتی بیوتیک جنتامایسین موجب افزایش ۵ برابری میزان مرگ و میر بیماران مبتلا به با کتریمی است.[5] فاکتور ویرولانس دیگر، ماده تجمع دهنده (aggregation substance) است که توسط پلاسمید کد میشود.[6]
مقاومت آنتی بیوتیکی
انتروکوک فکالیس به بیشتر آنتی بیوتیکها مانند آمینو گلوکوزیدها، آزترئونام، سفالوسپورینها، کلیندامایسین و پنی سیلینها مقاوم است.[7] مقاومت به وانکومایسین در انتروکوکها شایع تر بوده و از اهمیت ویژهای برخوردار است. از لینزولید و داپتومایسین برای درمان سویههای مقاوم به وانکومایسین استفاده میشود. کوئینوپریستین/دالفوپریستین (سینرسید) برای درمان انتروکوک فاسیوم و نه انتروکوک فکالیس استفاده میشود.[8]
سطح ضدباکتریایی آلیاژهای مس
با آزمایشهای بسیار، نشان داده شده است که سطح مس و آلیاژهای آن، باکتری انتروکوک فکالیس مقاوم به وایکومایسین (VRE) را در کمتر از ۲ ساعت از زمان آلودگی نابود میکند. این نتایج، نویدبخش غلبه بر عفونتهای بیمارستانی است. استفاده از مس در قسمتهای فلزی تخت و میز بیمار، شیرآلات و دستگیره درها، سینی، سینک و غیرو، به ویژه در بخش مراقبتهای ویژه بیمارستانها، سبب کاهش انتقال باکتری به دیگر افراد خواهد شد.[9]
منابع
- Ryan KJ, Ray CG (editors) (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 294––5. ISBN 0-8385-8529-9.
- «نسخه آرشیو شده». بایگانیشده از اصلی در ۶ ژوئیه ۲۰۱۲. دریافتشده در ۱۳ سپتامبر ۲۰۱۲.
- Molander A, Reit C, Dahlen G, Kvist T: Microbiological status of root-filled teeth with apical periodontitis, Int Endod J 31:1, 1998
- Murray, BE. (Jan 1990). "The life and times of the Enterococcus.". Clin Microbiol Rev 3 (1): 46–65. PMID 2404568.
- Huycke, MM. ; Spiegel, CA. ; Gilmore, MS. (Aug 1991). "Bacteremia caused by hemolytic, high-level gentamicin-resistant Enterococcus faecalis.". Antimicrob Agents Chemother 35 (8): 1626–34. PMID 1929336.
- Chow, JW. ; Thal, LA. ; Perri, MB. ; Vazquez, JA. ; Donabedian, SM. ; Clewell, DB. ; Zervos, MJ. (Nov 1993). "Plasmid-associated hemolysin and aggregation substance production contribute to virulence in experimental enterococcal endocarditis.". Antimicrob Agents Chemother 37 (11): 2474–7. PMID 8285637.
- Amyes SG (May 2007). "Enterococci and streptococci". Int. J. Antimicrob. Agents 29 Suppl 3: S43–52. doi:10.1016/S0924-8579(07)72177-5. PMID 17659211.
- Arias, CA. ; Contreras, GA. ; Murray, BE. (Jun 2010). "Management of multidrug-resistant enterococcal infections.". Clin Microbiol Infect 16 (6): 555–62. doi:10.1111/j.1469-0691.2010.03214.x. PMID 20569266.
- %7B%7Bیادکرد وب}}