وستیت
وستیت (Wustite) یک ماده معدنی ایجاد شده از آهن(II) اکسید است که در شهاب سنگها یافت شده. رنگ خاکستری مایل به سبز در نور بازتاب شده دارد. وستیت در مقیاس سختی موهس بین 5 تا 5.5 قرار میگیرد و چگالی نسبی آن 5.88 است. وستیت یک نمونه معمولی از ترکیب غیر استوکیومتری میباشد.
| وستیت | |
|---|---|
| اطلاعات کلی | |
| ردهبندی | Oxide minerals |
| فرمول شیمیایی (بخش تکراری) | FeO |
| دستهبندی شرونتس-نیکل | 4.AB.25 |
| دستگاه بلوری | Cubic |
| ویژگیها | |
| رنگ | Greyish white to yellow or brown; colorless in thin section |
| رفتار بلوری | Pyramidic, prismatic |
| رَخ | {001} perfect |
| شکستگی | Subconchoidal to rough |
| سختی موس | 5 - 5.5 |
| وزن مخصوص | 5.88 |
| چگالی | 5.7 g/cm3 |
| ضریب شکست | 1.735 to 2.32 in synthetic crystals |
| Pleochroism | None |
| انحلالپذیری | Soluble in dilute HCl |
| دیگر ویژگیها | Forms solid solution with periclase |
وستیت به خاطر فریتز ووست (Fritz Wust)، یک متالوژریست آلمانی و مدیر عامل Kaiser-Wilhelm-Institut für Eisenforschung نام گذاری شد.
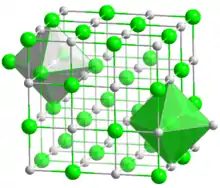
وستیت در طبیعت وجود ندارد و به عنوان کانی آهن معرفی نمیشود اما چون در مراحل نهایی احیای آهن تشکیل میشود لذا شناخت خصوصیات آن برای درک درست فرایند احیا لازم است. اگر چه اغلب فرمول شیمیایی این اکسید را به صورت FeO می نویسند ولی در واقع مقدار اکسیژن وستیت همیشه بیش از مقدار استوکیومتری است در نتیجه فرمول شیمیایی آن را میتوان به صورت Fe 1-xO نوشت، شبکه کریستالی وستیت مکعبی (شبکه آن مانند شبکه کلرید سدیم است) میباشد که در آن شبکه آهن ناقص بوده و جاهای خالی در شبکه وجود دارد. جهت خنثی شدن شبکه لازم است به ازای هر جای خالی آهن دو ظرفیتی، دو یون آهن سه ظرفیتی در شبکه وجود داشته باشد. مقدار X در فرمول شیمیایی وستیت بر حسب شرایط (مثلاً درجه حرارت) بین 0.175 تا 0.05 درصد تغییر میکند. با افزایش درجه حرارت تعداد جاهای خالی در شبکه وستیت افزایش می یابد. بنابراین درصد اکسیژن و تعداد یونهای سه ظرفیتی نیز افزایش می یابد. در دمای 1524 درجه سانتی گراد در نقطه C نمودار پایداری اکسیدهای آهن، آهن مذاب اشباع از اکسیژن در تعادل با یک فاز مایع نامحلول اکسید آهن دو ظرفیتی است که حاوی 22.6 درصد اکسیژن است. دمای ذوب این اکسید با افزایش اکسیژن کاهش می یابد و در دمای 1371 درجه سانتیگراد که کمترین مقدار دمای ذوب را دارد، در تعادل با آهن آستنیت جامد اشباع از اکسیژن است. بعد از آن دمای ذوب اکسید آهن دو ظرفیتی با زیاد شدن مقدار اکسیژن افزایش می یابد. از نمودار تعادلی دما - اکسیژن مشخص میشود اکسید آهن دو ظرفیتی که حاوی 22.6 درصد اکسیژن است و به صورت FeO نشان داده میشود وجود خارجی ندارد. مقدار متوسط اکسیژن در محدوده دمایی 1371-600 درجه سانتی گراد برای وستیت اشباع از آهن، برابر 23.2 درصد است بنابراین، فرمول شیمیایی وستیت در این محدوده دمایی FeO 0.95 یا FeO 1.05 است. تنها برای راحتی محاسبات فرمول شیمیایی وستیت را به صورت FeO می نویسند.
حضور اون باعث ایجاد یک محیط اکسایش کاهش شدید میباشد
بافر اکسایش کاهش وستیت
وستیت در ژئوشیمی، یک بافر اکسایش کاهش در میان سنگها در نقطهای که سنگ آنقدر کاهش یافته که Fe3 و بنابراین هماتیت، غایب هستند بهشمار میآید.
تأثیرات بر روی مواد معدنی سیلیکاتی
نسبت Fe2+ به Fe3+ در یک سنگ تعیینکننده میزان ماده معدنی سیلیکات در ساختار سنگ میباشد.در یک سنگ که ترکیبات شیمیایی آن داده شدهاست، آهن وارد مواد معدنی بر پایه ساختار شیمیایی اکثریت میشود و فازهای معدنی که در آن دما و فشار پایدار هستند میشود. آهن تنها میتواند وارد مواد معدنی ای از جمله پیروکسین و اولیوین شود اگر به صورت Fe2+ حضور داشته باشد. Fe3+ نمیتواند وارد شبکه فایالیت اولیوین شود و بنابراین برای هر دو یون Fe3+، یک Fe2+ استفاده شده و یک مولکول مگنتیت ساخته میشود.
در سنگهای شیمیایی کاهش یافته، مگنتیت ممکن است غایب باشد با توجه به گرایش آهن برای نفوذ به اولیوین، و وستیت تنها میتواند حاضر باشد اگر مقداری آهن بیش از آنچه که توسط سیلیکا استفاده میشود، وجود داشته باشد. بنابراین، وستیت تنها میتواند در ترکیباتی که سیلیکا در آنها کم است و به صورت شیمیایی بسیار کاهش یافته اند، حضور داشته باشد که هر دو نیاز حذف تمام Fe3+ و نگهداری آهن خارج از مواد معدنی سیلیکاتی را بر آورده کند.
در طبیعت، سنگهای کربنات، بهطور طبیعی کربوناتیت، کیمبرلیت ها، سنگهای کربنات بیرنگ ملیلیتیک و بقیه سنگهای آلکالین کمیابت شاید بتوانند این شروط را ارضا کنند. البته وستیت در اکثر این سنگها در طبیعت تابحال گزارش نشدهاست، در واقع به این دلیل که حالت اکسیداسیون مورد نیاز برای رساندن مگنتیت به وستیت بسیار کمیاب است.
تایخچه استفاده
طبق Vagn Fabritius Buchwald، وستیت یک جز مهم هنگام دوران آهن برای تسهیل کردن پروسه جوش کاری فورجینگ بود. در زمانهای قدیم، زمانی که آهنگری توسط یک کوره زغالی انجام می شد، گودال عمیق زغال سنگ که آهن یا فولاد در آن قرار می گرفتند، که یک مکان به شدت کاهشی را ایجاد میکرد، که همچنین مکان خالی از اکسیژنی بود، یک لایه نازک وستیت بر روی فلز ساخته می شد. در دمای جوش کاری، آهن بشدت با اکسیژن واکنش پذیر میشود، و جرقه می زند و لایههای کلفت از سرباره را هنگام مواجهه با هوا ایجاد میکند که جوش آهن یا فولاد را تقریباً غیرممکن میکند. برای حل این مشکل، آهنگران قدیم مقدار کمی شن را درون فلز سفید داغ می ریختند. سیلیکون موجود در شن آنگاه با وستیت واکنش می داد و فایالیت را شکل می داد که درست قبل از دمای ذوب، ذوب میشود. این یک فلاکس مؤثر را ایجاد میکرد که فلز را از اکسیژن محافظت میکرد و به استخراج اکسیژن و ناخالصیها کمک میکرد که یک سطح خالص را باقی می گذاشت که به راحتی میتوانست جوش بخورد. همچنین قدیمیان هیچ ایدهای از طرز کار این نداشتند. توانایی جوش کاری آهن به حرکت به سمت خروج از دوران برنز و ورود به دوران مدرن کمک کرد.
مواد معدنی مرتبط
وستیت یک محلول جامد با پریکلاس (MgO) میسازد. و آهن جایگزین منیزیم میشود. پریکلاس، وقتی که در آب حل میشود، بروسیت را شکل میدهد که یک محصول از واکنشهای سرپنتینیت متاموفیک است.
اکسیداسیون وستیت، گوتیت لمونیت را شکل میدهد.
روی، آلومینیم و دیگر فلزات امکان دارد با آهن در وستیت جایگزین شوند.
وستیت در اسکارنهای دولمیت امکان دارد به سیدریت (آهن - کربنات)، ولاستنیت، انستاتیت، دیپوسید و مگنسیت مرتبط شود.
