دگرشکلهای اکسیژن
چندین دگرشکل شناخته شده از اکسیژن وجود دارد. شناخته شدهترین آن اکسیژن مولکولی (O2) است، که در سطح قابل توجهی در جو زمین وجود دارد و همچنین به عنوان اکسیژن یا اکسیژن سهگانه شناخته میشود. ازون بسیار واکنش پذیر (O3) است. دیگر دگرشکلهای اکسیژن عبارتند از:
- اکسیژن اتمی (O 1)، یک ررادیکال آزاد است.
- اکسیژن منفرد (O 2 *)، یکی از دو حالت پایدار اکسیژن مولکولی است.
- Tetraoxygen (O 4)، یکی دیگر از اشکال قابل استفاده است.
- اکسیژن جامد، موجود در شش مرحله با رنگی مختلف که یکی از آنها O
8 {{سخ}} O
8 و دیگری فلزی است.
اکسیژن اتمی
اکسیژن اتمی، O (3 P) یا O (3P)، نشان داده میشود. بسیار واکنش پذیر است. در سطح زمین، مدت زمان طولانی بهطور طبیعی وجود ندارد، اما در فضای بیرونی، وجود مقدار زیادی پرتوهای فرابنفش در جو زمین مدار نزدیک زمین ایجاد میشود که در آن ۹۶٪ اکسیژن به شکل اتمی رخ میدهد.[1][2]
اکسیژن اتمی توسط برنامه فضایی مارینر، وایکینگ و رصدخانه استراتوسفری اخترشناسی فروسرخ در مریخ کشف شدهاست.[3]
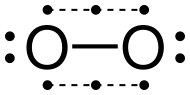
دیاکسیژن
آلوتروپ رایج اکسیژن عنصری در زمین، O۲ است که عموماً بهنام اکسیژن شناخته میشود و ممکن است برای متمایز کردن آن با عنصر اکسیژن و آلوتروپ سهاتمی اکسیژن، اوزون (O۳)، با نامهای دیاکسیژن، اکسیژن دواتمی، اکسیژن مولکولی یا گاز اکسیژن به آن اشاره شود.
منابع
- Ryan D. McCulla, Saint Louis University (2010). "Atomic Oxygen O(3P): Photogeneration and Reactions with Biomolecules".
- "Out of Thin Air". NASA.gov. February 17, 2011.